一、老年急性心肌梗死的临床特点
1. 临床症状不典型,合并危险因素(高血压、糖尿病、脑血管病、低体重)多,常合并其他脏器疾病(肿瘤、呼吸道、胃肠道、血液疾病及泌尿系感染等)。
➤特别是合并糖尿病的患者,临床表现常不典型,可表现为乏力、淡漠、单纯牙痛或背痛
➤部分患者患者下壁、右室心梗发作时,出现血压下降、缓慢性心律失常,影响脑灌注,临床上出现反复发作的黒矇、意识丧失等,易被认为是脑供血不足、TIA或脑梗死等缺血性脑血管病发作
➤急性下壁心肌梗死老年患者,因刺激膈肌,患者会有恶心、呕吐、腹泻等消化道症状
➤其他症状还包括晕厥、大汗、呼吸困难、休克等
2. 老年人受昼夜节律影响更大,以清晨6点至中午(12点)发作居多,可能与体内儿茶酚胺水平变化有关;受天气和气候变化影响,季节交替和遇冷空气时发作多。
3. 老年AMI患者中,猝死、重症心衰、恶性心律失常、心脏骤停的发生率升高;在全球心梗工作组的AMI分型中,I型和III型更常见。
4. 高龄患者冠脉病变复杂,介入治疗风险高,例如多支病变、弥漫病变、迂曲病变、钙化病变、CTO病变以及CABG术后病变(桥血管病变、原位病变)等。随着年龄增加,动脉粥样硬化及钙化病变越严重,GRACE评分增高,出血风险升高。
5. 治疗效果差,死亡率高。研究显示,年龄超过80岁的AMI患者多支病变、左室功能不全多,常合并外周、脑血管病及肾功能不全,PCI操作成功率低,复合终点(死亡、MI、卒中)事件发生率高。
二、老年急性心肌梗死的病理生理特点和发病机制
傅向华教授强调,STEMI病理生理和发病机制的关键是急性冠脉红血栓形成。冠脉粥样硬化是急性心梗的基本病因,冠脉易损板块破裂是STEMI的启动因素;凝血酶激活,红血栓不断发展造成血管闭塞。
血栓的三要素包括血管、凝血因子和血小板,凝血酶是三者的纽带,可催化纤维蛋白的生成、诱发血小板聚集。
血栓负荷决定梗死面积和患者预后。干预越早,血栓负荷小,冠脉越容易开通,无复流发生几率越小。因此,早期阻断血栓的发展是治疗的关键。
三、老年急性心肌梗死的诊治误区
误区一:症状不典型,易误诊、漏诊
1. 老年患者症状不典型,心梗早期诊断困难:老年人思维认知、反应能力及表达能力较差,不能准确描述症状;对疼痛的感知能力也较差,导致就诊延迟。
2. 老年急性心梗救治特点:发病至就诊时间长;D2B时间超过90min居多;病情复杂,合并症多,需多脏器综合评估。
误区二:对溶栓治疗重视程度不够
STEMI病理生理过程决定其治疗有时间迫切性和有效性。时间就是心肌,时间就是生命,特别是早期,时间是大片心肌!缩短总缺血时间极为重要,治疗要围绕时间和措施可行的原则。
傅向华教授指出,针对我国的AMI救治体系,宏观上要PCI和溶栓一起抓,基层溶栓更应是首选。溶栓具有早、快、易、廉、好的优点,大中小血栓、正向逆向都能溶,对微循环血栓也可以。开通血管是为了恢复有效的心肌微循环灌注,在这点上溶栓有其现实的病理和病理生理学意义的,也符合中国的AMI救治现状。
有人认为溶栓出血风险高,第一代纤溶酶(尿激酶、链激酶)为非靶向药物,出血风险较高,而新一代靶向药物出血风险大大降低,溶栓的再通率非常高。最新的ESC指南提出在确诊后10min内溶栓。
对于老年心梗患者,应尽早完成再灌注治疗,避免心肌进一步坏死;如时间条件允许,尽可能选择直接PCI;若医院无PCI条件、颅内出血危险低着可予以溶栓治疗或就近转诊至有条件的医院行急诊PCI;尽早完成缺血/出血风险评估,对于老年患者,需根据体重、肾功能等选择半量或更小剂量的溶栓药物。
误区三:溶栓治疗欠规范
1. 选择非特异性纤溶酶原激活剂(例如,尿激酶),溶栓再通率低,出血并发症高,使患者失去救治黄金窗口机会。
2017ACC STEMI指南和2015年中国STEMI指南均推荐采用特异性纤溶酶原激活剂进行溶栓治疗(I,B),不推荐采用非特异性纤溶酶原激活剂。
2. 只溶栓,轻抗凝;只溶栓,不抗凝。
肝素应该是第一时间首先给予的药物。STEMI患者溶栓后,如未予充分抗凝、抗血小板治疗,会导致血小板和凝血系统的反跳性激活,形成“继发性易损血液”,血液更粘,血栓顽固,不易疏通。若肝素应用剂量和疗程不充分,不但再通效果差,而且反弹高凝,会导致冠脉闭塞率增高。
抗凝抗栓是溶栓的基础,溶栓应在有效的抗凝抗栓基础上进行。溶栓前肝素化,血管开通率高;溶栓后肝素化,冠脉闭塞率低;PCI时肝素化,血栓负荷轻,无复流发生少。

肝素使用的两个误区:
(1)过分担心肝素导致的出血并发症和诱导的血小板减少症(HIT)
➤目前STEMI急诊介入治疗多选择桡动脉路径,其出血并发症发生率较股动脉路径时期已经明显减少
➤检测APTT/ACT,使APTT/ACT控制在基础值的1.5-2倍,可降低出血发生率
➤HIT发生率约1%,且常与所用肝素剂量相关,多在停药后逐渐恢复正常
➤第一支肝素很少引起出血并发症和HIT
(2)以低分子肝素替代普通肝素
目前,只有依诺肝素在STEMI救治中有循证医学证据,但前提是需要静脉30mg继以每12小时皮下注释1mg/kg。
依诺肝素可作为STEMI稳定期抗凝替代桥接治疗药物。
3. 忽视溶栓治疗结合PCI的应用
溶栓治疗结合PCI,可尽早行再灌注治疗,既缩短总缺血时间(时间优势),又保证后续开通效果(效果优势),实现双赢。
2017年ESC年会上,我国何奔教授报告了EARLY-MYO研究结果。该研究比较了溶栓后早期介入治疗(AF-PCI)和直接介入治疗(PPCI)两种治疗策略对发病6h内、介入治疗相关延迟超过1h的STEMI患者的疗效和安全性;数据显示,与现有指南推荐的优先直接介入治疗相比,先给予半量阿替普酶溶栓、溶栓成功后3-24小时行PCI,两者有相似的疗效和安全性,先溶栓再介入甚至比直接介入治疗获得了更好的心肌再灌注水平,临床硬终点也有改善的趋势。

误区四:缺乏整体意识,不能认识AMI短板效应
溶栓是再灌注治疗的开始而不是结束。STEMI患者溶栓后,应在3~24小时内转到上级PCI医院行冠脉造影检查,评估血管开通效果;如果溶栓后再通指标不明确或溶栓失败,应尽早转到上级PCI医院行冠脉造影和(或)PCI。
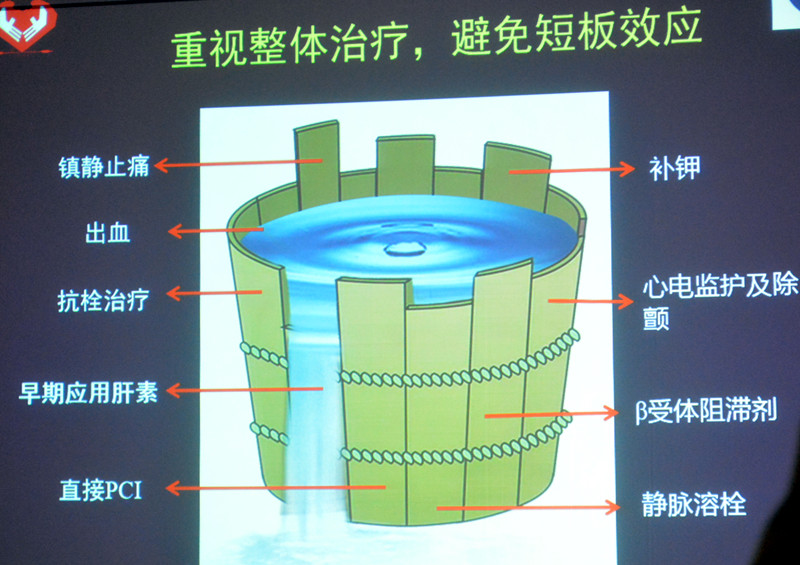
STEMI救治是一个系统工程,包括:(1)基础治疗:镇静、止痛、防猝死(室速/室颤——β受体阻滞剂+补钾);(2)主体治疗:即刻肝素化抗凝治疗,即刻抗血小板治疗(阿司匹林、替格瑞洛/氯吡格雷,必要时替罗非班);(3)关键再通治疗:①溶栓治疗——首选特异性纤溶酶原激活剂(阿替普酶、瑞替普酶、尿激酶原),②PCI治疗——120min内完成,若不能在FMC后120min内完成则先溶栓再转运造影或PCI,③再灌注治疗前、中、后冠脉微循环保护,防治并发症,减少早期心源性猝死。
STEMI救治需重视整体治疗,避免短板效应,任何一种治疗缺憾都可能导致整体治疗的失败。
AMI中左主干闭塞、前降支近段闭塞以及右冠口闭塞,容易发生低血钾性恶性心律失常;若对低血钾AMI患者行冠脉介入治疗,更容易因导管刺激诱发室速和室颤。STEMI合并低血钾患者中随血钾水平降低,室颤发生危险性显著增加。血钾水平<3.0mmol/L的患者室颤发生率达30%。
医生如仅仅注重心律失常本身及抗心律失常药物的应用,而忽视钾离子在心律失常发生和治疗中的重要作用,是导致治疗无效、原有心律失常加重或致心律失常发生的重要原因。
对于AMI患者的血钾水平,怎么重视都不过分,需防治低血钾,适时保持血钾的正常高限水平。
最有效的治疗方法为:静脉近心端(途径最好选择锁骨下静脉)的快速补钾,补镁(血钾应维持在4.5 mmol/L以上,血镁维持在1 mmol/L以上),同时加用静脉β受体阻滞剂(美托洛尔、艾司洛尔等)以提高室颤阈值,降低恶性心律失常的发生。
补钾加用β受体阻滞剂是抗心律失常的基础。在积极纠正低血钾的同时静脉应用β受体阻滞剂可降低交感张力,减少钾离子的细胞内转移,提高室颤阈值,从而预防室颤复发,减少恶性心律失常和猝死的发生。国内外指南对STEMI患者早期应用β受体阻滞剂均为I类推荐。
临床对老年患者不敢用β受体阻滞剂,但对心梗者,应该用,因其提高室颤阈的作用显著,可多重角度保护心肌。
总结(Take home message)
➤老年急性心梗症状常不典型,易漏诊、误诊,且危险因素和合并症多,治疗效果差,死亡率高
➤老年急性心梗应尽量缩短总缺血时间,尽早恢复有效心肌再灌注,根据血栓和出血风险评分选择合适的再灌注策略
➤建议选择直接介入干预,但时间条件不允许时可考虑溶栓,并结合患者情况半量或减量溶栓药物,控制抗凝抗栓力度
•重视早期肝素化,早期第一时间肝素很重要,FMC-H是关键基础治疗,老年也一样
•优先选择特异性纤溶酶原激活剂,配合有效的抗凝抗栓治疗
•半量溶栓结合PCI,溶栓后应在3-24h内行冠脉造影/PCI
➤重视整体治疗、避免短板效应,早期应用β受体阻滞剂,积极补钾,防猝死





