2017年11月是全球肺癌宣传月,盘点肺癌最新研究进展
时间:2017-11-29 09:38:14 来源:生物谷 点击:
肺癌是目前世界上死亡率最高的癌症之一,而且这一数字还在不断上升。这一现象背后的主要原因之一是针对肺癌的早期诊断效果不佳:患者在被诊断患有肺癌之后往往只能够存活5年的时间。另外一个问题在于肺癌存在很多不同的亚型,每一种亚型都对应有不同的治疗方案,因此需要对肺癌具备充分的理解才能够达到有效治疗的目的。
肺癌导致的癌症死亡的人数最多,据估计2012年全球有160万人死于肺癌,在不同类型的肺癌中,非小细胞肺癌(NSCLC)最为流行,最新的遗传学分析或能帮助研究人员开发治疗肺癌的新型靶向疗法,这种靶向疗法能够治疗携带特殊靶向突变的肺癌患者;另外一种有潜力的疗法则主要关注对机体免疫反应重新定向来使其识别并且攻击肿瘤细胞;尽管存在很多有潜力的方法,但研究人员仍然需要进行更多研究来理解引发肺癌进展的肿瘤动态学变化机制。
从1985年以来,肺癌已成为全球发病率和死亡率最高的恶性肿瘤,已成为一个严重的公共健康问题。世界卫生组织的报告显示,全球每年新发肺癌患者180万,死亡人数160万。2017年最新统计显示,新发肺癌人数达到80万,是我国名副其实的“第一癌症”!由此推算,肺癌发病率正以每年26.9%的速度增长,预计到2025年,我国每年仅死于肺癌的人数将接近100万人。据美国癌症协会数据显示,2017年在美国大约有222500新发肺癌病例,而且因肺癌死亡的患者数量为155870,80%至85%的肺癌患者都是NSCLC患者。
国际肺癌关注月是世界肺癌联盟在2001年发起的一项全球性倡议,目的是呼吁世界各国重视肺癌的预防,提高人们对肺癌的防癌、抗癌意识,普及肺癌的规范化诊疗知识。这一呼吁得到了世界上许多国家的响应,把每年的11月定为“国际肺癌关注月”。其下属国际癌症研究机构17日发布报告,首次指认大气污染“对人类致癌”,并视其为普遍和主要的环境致癌物, 后把11月17日定为国际肺癌日。
基于此,针对近来肺癌研究取得的最新进展,小编进行一番梳理。
1.Nature:重磅!蛋白NFS1让肺癌细胞免受铁凋亡
doi:10.1038/nature24637
 在一项新的研究中,来自美国纽约大学医学院等研究机构的研究人员发现阻断一种蛋白可释放出氧气来破坏肺癌细胞和乳腺癌细胞中的铁依赖性蛋白,从而延缓它们的生长并让它们更容易被杀死。相关研究结果于2017年11月22日在线发表在Nature期刊上,论文标题为“NFS1 undergoes positive selection in lung tumours and protects cells from ferroptosis”。
在一项新的研究中,来自美国纽约大学医学院等研究机构的研究人员发现阻断一种蛋白可释放出氧气来破坏肺癌细胞和乳腺癌细胞中的铁依赖性蛋白,从而延缓它们的生长并让它们更容易被杀死。相关研究结果于2017年11月22日在线发表在Nature期刊上,论文标题为“NFS1 undergoes positive selection in lung tumours and protects cells from ferroptosis”。
人细胞含有48种已知依赖于铁硫簇发挥功能的蛋白。一旦遇到氧气,这些铁硫簇就会降解,因此如果正常的细胞要在肺部等高氧环境中存活下来,那么它们就必须不断地替换这些受到降解的铁硫簇,而且如果肺癌细胞想要异常快地生长的话,它们应更加快速地替换这些铁硫簇。这项新的研究证实肺腺癌细胞通过产生更多的蛋白NFS1而在这种氧气威胁中存活下来。这种蛋白从半胱氨酸中收集更多的硫元素用于产生铁硫簇。这些研究人员还发现已扩散到肺部的乳腺癌细胞一进入这种种高氧环境中就促进NFS1产生,而当它们在乳腺中时则不会如此。
这些研究人员说,从两种角度而言,NFS1可能对肺癌细胞的存活是至关重要的。他们发现如果NFS1的活性不足以跟上氧气介导的铁硫簇破坏,那么癌细胞会耗尽产生重要的蛋白所需的这些关键性构成元件(即铁硫簇),因而停止增殖。或者,铁硫簇的数量可能用作检测铁水平的传感器。当这些铁硫簇的水平过低时,细胞“认为”它们缺乏铁,因而就从储存它的分子中释放出更多的铁。在对体外培养的癌细胞的研究中,这些研究人员发现这种“游离”铁的堆积会导致活性氧(ROS)产生,而ROS会破坏细胞膜,并导致一种被称作铁凋亡(ferroptosis)的细胞死亡。他们指出在未来还需在活动物体内开展进一步的研究来证实这一点。
2.Cell:揭示HLA基因杂合性丢失让非小细胞肺癌逃避免疫系统破坏
doi:10.1016/j.cell.2017.10.001
根据在2017年10月26日~30日举办的美国癌症研究协会(AACR)-美国国家癌症研究所(NCI)-欧洲癌症治疗研究组织(EORTC)国际分子靶标与癌症治疗会议(International Conference on Molecular Targets and Cancer Therapeutics)上提供的数据,在分析的40%的非小细胞肺癌(NSCLC)病例中检测到一种特定的基因变化允许癌细胞逃避免疫系统检测。这些数据提示着这种基因变化是在肿瘤进化的晚期发生的。相关研究结果于2017年10月26日在线发表在Cell期刊上,论文标题为“Allele-Specific HLA Loss and Immune Escape in Lung Cancer Evolution”。论文通信作者为英国伦敦大学学院癌症研究所的Charles Swanton博士和Nicholas McGranahan博士。
Swanton实验室研究生Rachel Rosenthal说,“癌症的一种特征是癌细胞能够逃避免疫系统破坏。通过与McGranahan博士一起,我们开发出一种方法来分析我们是否在肺癌中观察到一种潜在的免疫逃避机制---人白细胞抗原(human leukocyte antigen, HLA)位点的杂合性丢失(loss of heterozygosity, LOH),以及如果我们发现它发生的话,研究它的发生率和它如何可能影响肿瘤进化。”
这些研究人员获得90名登记参加TRACERx(tracking cancer evolution through therapy, 通过治疗追踪癌症进化)研究的NSCLC患者在治疗前的肿瘤样品,并利用LOHHLA分析了来自这些肿瘤样品的下一代测序数据。他们在40%的患者中检测到HLA LOH。
3.Sci Trans Med:肺癌会导致肺动脉高压症状的发生
doi:10.1126/scitranslmed.aai9048
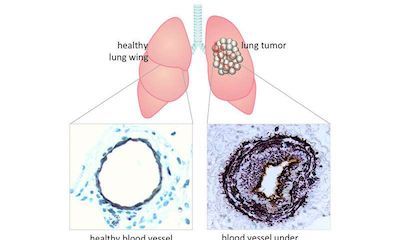 呼吸不畅往往会增加晚期肺癌患者的痛苦,这主要是由于肺动脉高压症状导致的。最近,来自马普的研究者们通过对500名患者进行研究,发现肺动脉高压的症状主要是由于癌细胞驱动的免疫与炎症反应导致的,因此对应的治疗手段或许可以改善这一症状。
呼吸不畅往往会增加晚期肺癌患者的痛苦,这主要是由于肺动脉高压症状导致的。最近,来自马普的研究者们通过对500名患者进行研究,发现肺动脉高压的症状主要是由于癌细胞驱动的免疫与炎症反应导致的,因此对应的治疗手段或许可以改善这一症状。
医生们已经发现许多晚期肺癌患者会产生呼吸不畅的症状,这一症状与肺动脉高压的症状相似。来自马普的研究者们因此检测了500名肺癌患者的肺动脉直径。“我们发现超过一半的患者肺动脉出现了增厚的现象,这解释了为什么一半以上的患者会出现肺动脉高压的症状”,该研究的首席作者Rajkumar Savai说道。
那么究竟为什么肺癌会导致肺动脉高压症状的产生呢?小鼠以及人源样本中均没有检测到血管中存在的癌细胞或结块。然而,研究者们发现肿瘤附近的血管浸润了大量的免疫细胞。进一步的研究则发现这些免疫细胞能够释放多种化学信号分子,类似于炎症反应的发生过程。相反地,在免疫系统缺陷的小鼠中,作者并没有发现血管壁增厚的现象。这些结果表明肺癌细胞引发的炎症反应或许是导致肺动脉高压症状产生的原因。
4.Sci Rep:重磅!科学家有望开发出抑制肺癌进展的新型疗法
doi:10.1038/s41598-017-04097-7
最近,一篇发表在Scientific Reports杂志上的研究报告中,来自肯塔基大学的研究人员通过研究揭示了一种新型的细胞信号相互作用,其或能有效帮助抑制肺癌进展的关键步骤。
这项研究中,研究人员进行通力合作,旨在解决上述问题,此前研究者通过研究发现了一系列microRNAs分子或许能够帮助预测非小细胞肺癌对药物埃罗替尼的敏感性,埃罗替尼是一种能有效治疗特定患者肺癌的药物;microRNAs分子是一种小型RNA分子,其在调节机体诸如细胞生长和增殖等生物学过程中扮演着关键角色。
本文研究中,当研究者对microRNA基因进行深入研究后他们发现了转化生长因子TGFβ在开启肺癌转移和表皮生长因子受体(EGFR)信号的非小细胞肺癌之间的一种新型关联,microRNA分子能够改变TGFβ的活性,从而抑制癌症的上皮-间质转化过程,而这种相互作用同时也需要EGFR的活性,或许在癌症开始发生转移时这种过程并未被研究者所注意到。
5.Sci Rep:突破!科学家鉴别出肺癌免疫疗法新靶点!
doi:10.1038/s41598-017-09928-1
近日,一项刊登在国际杂志Scientific Reports上的研究报告中,来自瑞士伯尔尼大学医院等机构的研究人员通过研究发现,来自肺部肿瘤中的血管周样细胞会表现地行为异常,其不仅会不恰当地支持血管结构,而且还会积极调节机体炎症和免疫反应,相关研究或为研究人员开发治疗间质癌症的新型疗法提供新的靶点。
文章中,研究者发现,血管周细胞在肿瘤的进展过程中扮演着关键的角色,这或为研究人员能够提供新型免疫疗法的靶点。研究者Sean Hall说道,目前越来越多的证据都认为血管周细胞和肿瘤发生发展之间存在一定关联,这也就是为何我们要开展这项研究的原因;这项研究中,我们对进行胸外科手术的NSCLC患者的样本进行了收集,随后在实验室中我们对这些肺癌样本中的血管周细胞进行分离。
相比来自正常肺部组织的相同细胞类型而言,来自NSCLC患者机体中的血管周细胞往往会表现出多种异常特性,其中一种名为白介素-6的促炎细胞因子表达上升了,白介素-6就是一种PD-L1,而PD-L1是一种可命中目标的靶向性免疫检查点抑制剂;相关研究结果表明,非小细胞肺癌患者机体中的血管周细胞能够积极调解机体的炎症和免疫反应。
6.JAMA Inter Med:吸烟会提高HIV患者因肺癌死亡的风险
doi:10.1001/jamainternmed.2017.4349
 根据来自麻省总医院的研究者们的最新成果,接受抗逆转录疗法的HIV患者如果有吸烟习惯的话,他们因癌症死亡的几率会比HIV本身的致死率高10倍之多。这项研究发表在最近一期的《JAMA Internal Medicine》杂志上。
根据来自麻省总医院的研究者们的最新成果,接受抗逆转录疗法的HIV患者如果有吸烟习惯的话,他们因癌症死亡的几率会比HIV本身的致死率高10倍之多。这项研究发表在最近一期的《JAMA Internal Medicine》杂志上。
利用计算机进行建模与模拟分析,研究者们基于患者吸烟的情况估计了目前美国境内HIV患者患肺癌的风险。其它一些疾病,例如心脏病等等,也被列入的估计的范围。
研究者们发现, HIV患者在接受抗逆转录药物治疗之后继续保持吸烟习惯的会有25%的死亡率,而对于40岁之前戒烟的患者来说,因肺癌死亡的风险仅有6%。此外,研究者们还发现有吸烟习惯的HIV患者在接受抗逆转录治疗之后因肺癌死亡的几率是HIV致死率的6到13倍。
7.Sci Signal:重磅!科学家成功鉴别出抵御肺癌的新型靶点!
doi:10.1126/scisignal.aam6291
近日,一项刊登在国际杂志Science Signaling上的研究报告中,来自波士顿大学医学院的研究人员通过研究在非小细胞肺癌癌细胞中鉴别出了一种名为miR-124的分子,该分子或在癌细胞的命运决定中扮演着调节性的角色,其能够帮助确定癌细胞的特殊亚型是否会经历程序性细胞死亡过程,相关研究或为后期研究人员开发抵御非小细胞肺癌的新型靶向疗法提供新的思路。
研究者表示,miR-124分子能够促进正在经历上皮细胞-间质细胞转化的特殊亚型的肺癌细胞发生程序性细胞死亡,这些间质样细胞中携带有名为KRAS的突变,其通常会对化疗制剂所产生的诱导死亡效应产生耐受反应。
通过对人类肺癌衍生细胞系进行分析,研究人员确定了两种肺癌细胞亚型的特性,当对比了生物化学特性后研究人员发现,名为miR-124的分子或许在级联放大信号中扮演着关键角色,这种信号能够帮助确定特殊类型癌细胞死亡还是存活。
8.Sci Transl Med:科学家发现β受体阻滞剂可阻断压力导致的肺癌耐药性,并抑制肿瘤生长
doi:10.1126/scitranslmed.aao4307
越来越多的研究表明,心理压力会促进癌细胞的生长、产生耐药性,以及转移。以至于临床将心理压力作为预测肺癌患者死亡风险的一个指标。
就拿非小细胞肺癌来说吧,它是发病率最高的癌症。近日,来自MD安德森癌症中心的Monique B. Nilsson团队发现,压力激素不仅会促进癌细胞的生长,还会促进癌细胞对治疗非小细胞肺癌的经典药物TKI抑制剂产生耐药性。更重要的是,这种现象不仅仅是在小鼠身上观察到的,她们回顾性的研究了一个III期临床研究的数据,初步证实β受体阻滞剂确实可以让肺癌患者受益。他们的这一重要研究成果刊登在著名期刊《科学转化医学》上。
9.清华大学医学院李海涛课题组《自然通讯》发表合作论文揭示 YEATS2 在非小细胞肺癌发生中的促癌作用
doi:10.1038/s41467-017-01173-4
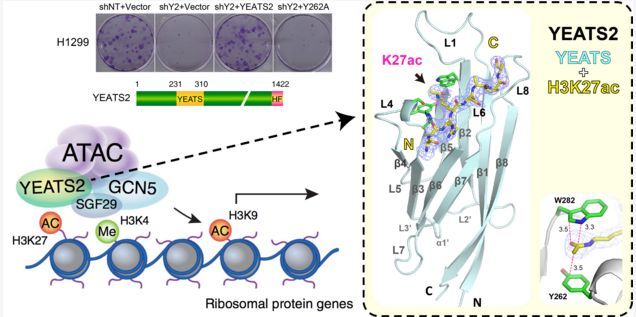 2017 年 10 月 20 日,生命中心李海涛研究组和美国德克萨斯大学安德森癌症中心石晓冰课题组合作于《自然通讯》(Nature Communications)发表题为“YEATS2 links histone acetylation to tumorigenesis of non-small cell lung cancer”(YEATS2 关联组蛋白乙酰化至非小细胞肺癌肿瘤发生)的研究论文。该论文发现酰基化“阅读器”蛋白 YEATS2 在非小细胞肺癌中高表达,通过识别组蛋白 H3 赖氨酸 27 乙酰化(H3K27ac)促进组蛋白 H3 赖氨酸 9 乙酰化(H3K9ac),进而维持下游核糖体基因的活跃转录并促进非小细胞肺癌发生。该研究首次报导了 YEATS2 的促癌作用,并揭示出一种染色质层面乙酰化信号放大机制,为 YEATS 家族蛋白在肿瘤发生中的机制研究提供了新线索。
2017 年 10 月 20 日,生命中心李海涛研究组和美国德克萨斯大学安德森癌症中心石晓冰课题组合作于《自然通讯》(Nature Communications)发表题为“YEATS2 links histone acetylation to tumorigenesis of non-small cell lung cancer”(YEATS2 关联组蛋白乙酰化至非小细胞肺癌肿瘤发生)的研究论文。该论文发现酰基化“阅读器”蛋白 YEATS2 在非小细胞肺癌中高表达,通过识别组蛋白 H3 赖氨酸 27 乙酰化(H3K27ac)促进组蛋白 H3 赖氨酸 9 乙酰化(H3K9ac),进而维持下游核糖体基因的活跃转录并促进非小细胞肺癌发生。该研究首次报导了 YEATS2 的促癌作用,并揭示出一种染色质层面乙酰化信号放大机制,为 YEATS 家族蛋白在肿瘤发生中的机制研究提供了新线索。
非小细胞肺癌是肺癌最常见的组织学类型,约占肺癌总数的 80-85%,近年来非小细胞肺癌发病率不断增高,无论是在我国还是全球,都已成为致死率最高的肿瘤。发表在《自然通讯》上的论文发现 YEATS2 基因在多种癌症细胞,尤其是非小细胞肺癌细胞中过量表达。研究者以非小细胞肺癌为研究体系,发现 YEATS2 基因敲低会明显抑制癌症细胞的增殖,随后的基因表达谱分析显示 YEATS2 可以上调一组核糖体编码基因(如 RPL7,PRL8,RPL35,RPL38 等)的表达,而这些基因对于维持细胞的正常生长十分重要。通过生化和结构生物学研究,李海涛课题组解析了 2.7 埃分辨率的 YEATS2 蛋白 YEATS 结构域特异性识别组蛋白 H3K27ac 的晶体结构,发现其 YEATS 结构域主要通过一种疏水的、丝氨酸内衬的三明治芳香笼口袋(S261、Y262、W282)实现对组蛋白 H3K27ac 侧链的精准识别,该识别涉及氢键、芳香 -π和碳氢 -π等相互作用,对其核心氨基酸进行突变则会明显减弱 YEATS 与组蛋白底物的结合能力。值得注意的是,YEATS2 存在于组蛋白乙酰转移酶 ATAC(Ada-Two-A-Containing)复合物中,该复合物可通过其催化亚基 GCN5 产生组蛋白 H3K9ac 修饰,从而提示一种从 H3K27ac 到 H3K9ac 的乙酰化放大机制。结合 ChIP-seq 和 ChIP-qPCR 分析,研究者们发现,ATAC 复合物和 H3K27ac 以及 H3K9ac 共定位于活跃转录基因的启动子区域,而 YEATS2 敲低明显减弱了 ATAC 复合物介导的下游靶基因(特别是核糖体基因)启动子区域 H3K9ac 的水平。进一步通过敲低 YEATS2 后过表达野生型 YEATS2 和阅读器口袋突变体,发现突变体无法挽救 ATAC 复合物依赖的核糖体基因的表达,同时也无法恢复癌症细胞的生长,从而证明了 YEATS2 对组蛋白乙酰化底物的识别对于非小细胞肺癌的发生、发展至关重要。
YEATS 结构域作为一类新型的组蛋白酰基化“阅读器”,其家族成员(YAF9,ENL,AF9,TAF14,SAS5 等)可形成多种复合物参与转录调控、组蛋白沉积、染色质重塑等过程。近年来,围绕 YEATS 家族蛋白识别组蛋白酰基化修饰的分子机制、及对其生物学功能的探索成为表观遗传领域的研究热点。该论文结合生物化学、细胞生物学、结构生物学等多种技术手段,展示了 YEATS2 通过介导组蛋白识别与催化而实现乙酰化信号放大的分子机制,并将 YEATS2 定义为一类促癌因子,为非小细胞肺癌等相关疾病的靶向治疗提供新思路。
10.Cancer Cell:科学家发现长期吸烟引起的肺细胞DNA表观遗传学变化或是肺癌发生的第一步
doi:10.1016/j.ccell.2017.08.006
近日,约翰霍普金斯大学研究人员给出了答案:香烟烟雾会导致细胞发生异常的DNA甲基化,进而使抑癌基因表达量下降,这会引起促进细胞生长的KRAS基因表达量升高,如果这个烟民的KRAS基因恰巧发生了致癌突变(1/3的吸烟肺癌患者携带这个突变),那么启动肺癌的第一步就这样开始了!
这项研究由约翰霍普金斯大学肿瘤学教授,Stephen Baylin,带领团队完成。最新的研究成果刊登在9月11日的著名学术杂志《Cancer Cell》上。
这些研究人员还发现只有暴露在烟草烟雾凝集物15个月的细胞(相当于人吸烟30年),在致癌突变的作用下,才能让小鼠长出肿瘤来,即发生致癌转化。而暴露在烟草烟雾凝集物6个月的细胞(相当于人吸烟12年),由于它的异常甲基化还不彻底,抑癌基因还可以发挥作用,所以即使是致癌的KRAS基因突变存在,细胞也不能发生致癌转化。
这些结果表明,慢性香烟烟雾暴露引起的早期表观遗传学变化,会随着时间的增加而增加,并且让人支气管上皮细胞对致癌的基因突变越来越敏感。它们和美国“癌症基因组图集”(TCGA)的数据分析结果不谋而合:与没有戒烟的人相比,戒烟10年以上的人的异常甲基化水平明显降低!
11.JNCI:周光飚研究组发现肺癌精准治疗新标记
doi:10.1093/jnci/djx157
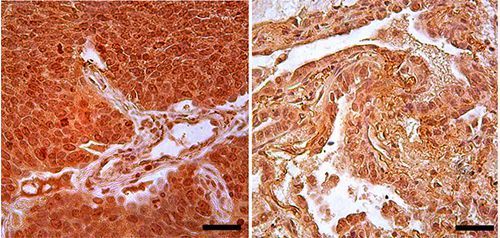 发现基因及其编码蛋白质的异常是癌症精准治疗的基础。局部黏着斑激酶(focal adhesion kinase, FAK)是一种重要的非受体型酪氨酸激酶,在几乎所有的细胞中均有表达,可将细胞外的重要信号(如细胞生长、营养等)向细胞内传导,调控细胞的基本生物学功能。FAK在肺癌等肿瘤中表达增高并与病人预后负相关,抑制FAK在临床试验中显示一定的抗癌活性。然而,目前缺乏指导FAK抑制剂临床应用的生物标记物。
发现基因及其编码蛋白质的异常是癌症精准治疗的基础。局部黏着斑激酶(focal adhesion kinase, FAK)是一种重要的非受体型酪氨酸激酶,在几乎所有的细胞中均有表达,可将细胞外的重要信号(如细胞生长、营养等)向细胞内传导,调控细胞的基本生物学功能。FAK在肺癌等肿瘤中表达增高并与病人预后负相关,抑制FAK在临床试验中显示一定的抗癌活性。然而,目前缺乏指导FAK抑制剂临床应用的生物标记物。
动物研究所周光飚研究组系统研究了非小细胞肺癌中FAK的结构变异体。他们对91例肺癌病人的FAK基因组序列和编码区序列进行测序,发现在7例病人癌组织中存在4种类型的FAK变异体:一例病人发生基因内部串联重复突变体(FAK-ITD),一例病人发生A1004S点突变,一例病人发生第5-27号外显子缺失的突变,四例病人表达剪切异构体FAK6,7(在Y397自磷酸化位点前后分别插入编码6、7个氨基酸的外显子Box 6和Box 7)。与不吸烟病人相比,吸烟病人发生FAK变异的比例明显增高。分析癌症基因组测序TCGA数据库中肺癌病人的RNA测序数据,发现在508例肺腺癌病人中有42例 (占8.3%)、501例肺鳞癌病人中有37例 (占7.4%)病人表达含有“Box 6”及/或“Box 7”的 FAK可变剪切变异体,且吸烟的肺腺癌病例发生FAK结构变异的比例明显高于非吸烟病人。与野生型FAK相比, FAK-ITD和FAK6,7的自磷酸化水平增强(见图),酪氨酸激酶活性增高,对FAK激酶抑制剂的敏感性显著增强。该研究对肺癌病人FAK 抑制剂的临床精准应用具有指导意义,也说明吸烟可引起重要基因的剪切变异从而危害健康。 这一研究成果日前发表在Journal of the National Cancer Institute期刊上。
肺癌导致的癌症死亡的人数最多,据估计2012年全球有160万人死于肺癌,在不同类型的肺癌中,非小细胞肺癌(NSCLC)最为流行,最新的遗传学分析或能帮助研究人员开发治疗肺癌的新型靶向疗法,这种靶向疗法能够治疗携带特殊靶向突变的肺癌患者;另外一种有潜力的疗法则主要关注对机体免疫反应重新定向来使其识别并且攻击肿瘤细胞;尽管存在很多有潜力的方法,但研究人员仍然需要进行更多研究来理解引发肺癌进展的肿瘤动态学变化机制。
从1985年以来,肺癌已成为全球发病率和死亡率最高的恶性肿瘤,已成为一个严重的公共健康问题。世界卫生组织的报告显示,全球每年新发肺癌患者180万,死亡人数160万。2017年最新统计显示,新发肺癌人数达到80万,是我国名副其实的“第一癌症”!由此推算,肺癌发病率正以每年26.9%的速度增长,预计到2025年,我国每年仅死于肺癌的人数将接近100万人。据美国癌症协会数据显示,2017年在美国大约有222500新发肺癌病例,而且因肺癌死亡的患者数量为155870,80%至85%的肺癌患者都是NSCLC患者。
国际肺癌关注月是世界肺癌联盟在2001年发起的一项全球性倡议,目的是呼吁世界各国重视肺癌的预防,提高人们对肺癌的防癌、抗癌意识,普及肺癌的规范化诊疗知识。这一呼吁得到了世界上许多国家的响应,把每年的11月定为“国际肺癌关注月”。其下属国际癌症研究机构17日发布报告,首次指认大气污染“对人类致癌”,并视其为普遍和主要的环境致癌物, 后把11月17日定为国际肺癌日。
基于此,针对近来肺癌研究取得的最新进展,小编进行一番梳理。
1.Nature:重磅!蛋白NFS1让肺癌细胞免受铁凋亡
doi:10.1038/nature24637

图片来自James Heilman博士/Wikipedia。
人细胞含有48种已知依赖于铁硫簇发挥功能的蛋白。一旦遇到氧气,这些铁硫簇就会降解,因此如果正常的细胞要在肺部等高氧环境中存活下来,那么它们就必须不断地替换这些受到降解的铁硫簇,而且如果肺癌细胞想要异常快地生长的话,它们应更加快速地替换这些铁硫簇。这项新的研究证实肺腺癌细胞通过产生更多的蛋白NFS1而在这种氧气威胁中存活下来。这种蛋白从半胱氨酸中收集更多的硫元素用于产生铁硫簇。这些研究人员还发现已扩散到肺部的乳腺癌细胞一进入这种种高氧环境中就促进NFS1产生,而当它们在乳腺中时则不会如此。
这些研究人员说,从两种角度而言,NFS1可能对肺癌细胞的存活是至关重要的。他们发现如果NFS1的活性不足以跟上氧气介导的铁硫簇破坏,那么癌细胞会耗尽产生重要的蛋白所需的这些关键性构成元件(即铁硫簇),因而停止增殖。或者,铁硫簇的数量可能用作检测铁水平的传感器。当这些铁硫簇的水平过低时,细胞“认为”它们缺乏铁,因而就从储存它的分子中释放出更多的铁。在对体外培养的癌细胞的研究中,这些研究人员发现这种“游离”铁的堆积会导致活性氧(ROS)产生,而ROS会破坏细胞膜,并导致一种被称作铁凋亡(ferroptosis)的细胞死亡。他们指出在未来还需在活动物体内开展进一步的研究来证实这一点。
2.Cell:揭示HLA基因杂合性丢失让非小细胞肺癌逃避免疫系统破坏
doi:10.1016/j.cell.2017.10.001
根据在2017年10月26日~30日举办的美国癌症研究协会(AACR)-美国国家癌症研究所(NCI)-欧洲癌症治疗研究组织(EORTC)国际分子靶标与癌症治疗会议(International Conference on Molecular Targets and Cancer Therapeutics)上提供的数据,在分析的40%的非小细胞肺癌(NSCLC)病例中检测到一种特定的基因变化允许癌细胞逃避免疫系统检测。这些数据提示着这种基因变化是在肿瘤进化的晚期发生的。相关研究结果于2017年10月26日在线发表在Cell期刊上,论文标题为“Allele-Specific HLA Loss and Immune Escape in Lung Cancer Evolution”。论文通信作者为英国伦敦大学学院癌症研究所的Charles Swanton博士和Nicholas McGranahan博士。
Swanton实验室研究生Rachel Rosenthal说,“癌症的一种特征是癌细胞能够逃避免疫系统破坏。通过与McGranahan博士一起,我们开发出一种方法来分析我们是否在肺癌中观察到一种潜在的免疫逃避机制---人白细胞抗原(human leukocyte antigen, HLA)位点的杂合性丢失(loss of heterozygosity, LOH),以及如果我们发现它发生的话,研究它的发生率和它如何可能影响肿瘤进化。”
这些研究人员获得90名登记参加TRACERx(tracking cancer evolution through therapy, 通过治疗追踪癌症进化)研究的NSCLC患者在治疗前的肿瘤样品,并利用LOHHLA分析了来自这些肿瘤样品的下一代测序数据。他们在40%的患者中检测到HLA LOH。
3.Sci Trans Med:肺癌会导致肺动脉高压症状的发生
doi:10.1126/scitranslmed.aai9048

图片来源: MPI f. Heart and Lung Research。
医生们已经发现许多晚期肺癌患者会产生呼吸不畅的症状,这一症状与肺动脉高压的症状相似。来自马普的研究者们因此检测了500名肺癌患者的肺动脉直径。“我们发现超过一半的患者肺动脉出现了增厚的现象,这解释了为什么一半以上的患者会出现肺动脉高压的症状”,该研究的首席作者Rajkumar Savai说道。
那么究竟为什么肺癌会导致肺动脉高压症状的产生呢?小鼠以及人源样本中均没有检测到血管中存在的癌细胞或结块。然而,研究者们发现肿瘤附近的血管浸润了大量的免疫细胞。进一步的研究则发现这些免疫细胞能够释放多种化学信号分子,类似于炎症反应的发生过程。相反地,在免疫系统缺陷的小鼠中,作者并没有发现血管壁增厚的现象。这些结果表明肺癌细胞引发的炎症反应或许是导致肺动脉高压症状产生的原因。
4.Sci Rep:重磅!科学家有望开发出抑制肺癌进展的新型疗法
doi:10.1038/s41598-017-04097-7
最近,一篇发表在Scientific Reports杂志上的研究报告中,来自肯塔基大学的研究人员通过研究揭示了一种新型的细胞信号相互作用,其或能有效帮助抑制肺癌进展的关键步骤。
这项研究中,研究人员进行通力合作,旨在解决上述问题,此前研究者通过研究发现了一系列microRNAs分子或许能够帮助预测非小细胞肺癌对药物埃罗替尼的敏感性,埃罗替尼是一种能有效治疗特定患者肺癌的药物;microRNAs分子是一种小型RNA分子,其在调节机体诸如细胞生长和增殖等生物学过程中扮演着关键角色。
本文研究中,当研究者对microRNA基因进行深入研究后他们发现了转化生长因子TGFβ在开启肺癌转移和表皮生长因子受体(EGFR)信号的非小细胞肺癌之间的一种新型关联,microRNA分子能够改变TGFβ的活性,从而抑制癌症的上皮-间质转化过程,而这种相互作用同时也需要EGFR的活性,或许在癌症开始发生转移时这种过程并未被研究者所注意到。
5.Sci Rep:突破!科学家鉴别出肺癌免疫疗法新靶点!
doi:10.1038/s41598-017-09928-1
近日,一项刊登在国际杂志Scientific Reports上的研究报告中,来自瑞士伯尔尼大学医院等机构的研究人员通过研究发现,来自肺部肿瘤中的血管周样细胞会表现地行为异常,其不仅会不恰当地支持血管结构,而且还会积极调节机体炎症和免疫反应,相关研究或为研究人员开发治疗间质癌症的新型疗法提供新的靶点。
文章中,研究者发现,血管周细胞在肿瘤的进展过程中扮演着关键的角色,这或为研究人员能够提供新型免疫疗法的靶点。研究者Sean Hall说道,目前越来越多的证据都认为血管周细胞和肿瘤发生发展之间存在一定关联,这也就是为何我们要开展这项研究的原因;这项研究中,我们对进行胸外科手术的NSCLC患者的样本进行了收集,随后在实验室中我们对这些肺癌样本中的血管周细胞进行分离。
相比来自正常肺部组织的相同细胞类型而言,来自NSCLC患者机体中的血管周细胞往往会表现出多种异常特性,其中一种名为白介素-6的促炎细胞因子表达上升了,白介素-6就是一种PD-L1,而PD-L1是一种可命中目标的靶向性免疫检查点抑制剂;相关研究结果表明,非小细胞肺癌患者机体中的血管周细胞能够积极调解机体的炎症和免疫反应。
6.JAMA Inter Med:吸烟会提高HIV患者因肺癌死亡的风险
doi:10.1001/jamainternmed.2017.4349

图片来源:NIH。
利用计算机进行建模与模拟分析,研究者们基于患者吸烟的情况估计了目前美国境内HIV患者患肺癌的风险。其它一些疾病,例如心脏病等等,也被列入的估计的范围。
研究者们发现, HIV患者在接受抗逆转录药物治疗之后继续保持吸烟习惯的会有25%的死亡率,而对于40岁之前戒烟的患者来说,因肺癌死亡的风险仅有6%。此外,研究者们还发现有吸烟习惯的HIV患者在接受抗逆转录治疗之后因肺癌死亡的几率是HIV致死率的6到13倍。
7.Sci Signal:重磅!科学家成功鉴别出抵御肺癌的新型靶点!
doi:10.1126/scisignal.aam6291
近日,一项刊登在国际杂志Science Signaling上的研究报告中,来自波士顿大学医学院的研究人员通过研究在非小细胞肺癌癌细胞中鉴别出了一种名为miR-124的分子,该分子或在癌细胞的命运决定中扮演着调节性的角色,其能够帮助确定癌细胞的特殊亚型是否会经历程序性细胞死亡过程,相关研究或为后期研究人员开发抵御非小细胞肺癌的新型靶向疗法提供新的思路。
研究者表示,miR-124分子能够促进正在经历上皮细胞-间质细胞转化的特殊亚型的肺癌细胞发生程序性细胞死亡,这些间质样细胞中携带有名为KRAS的突变,其通常会对化疗制剂所产生的诱导死亡效应产生耐受反应。
通过对人类肺癌衍生细胞系进行分析,研究人员确定了两种肺癌细胞亚型的特性,当对比了生物化学特性后研究人员发现,名为miR-124的分子或许在级联放大信号中扮演着关键角色,这种信号能够帮助确定特殊类型癌细胞死亡还是存活。
8.Sci Transl Med:科学家发现β受体阻滞剂可阻断压力导致的肺癌耐药性,并抑制肿瘤生长
doi:10.1126/scitranslmed.aao4307
越来越多的研究表明,心理压力会促进癌细胞的生长、产生耐药性,以及转移。以至于临床将心理压力作为预测肺癌患者死亡风险的一个指标。
就拿非小细胞肺癌来说吧,它是发病率最高的癌症。近日,来自MD安德森癌症中心的Monique B. Nilsson团队发现,压力激素不仅会促进癌细胞的生长,还会促进癌细胞对治疗非小细胞肺癌的经典药物TKI抑制剂产生耐药性。更重要的是,这种现象不仅仅是在小鼠身上观察到的,她们回顾性的研究了一个III期临床研究的数据,初步证实β受体阻滞剂确实可以让肺癌患者受益。他们的这一重要研究成果刊登在著名期刊《科学转化医学》上。
9.清华大学医学院李海涛课题组《自然通讯》发表合作论文揭示 YEATS2 在非小细胞肺癌发生中的促癌作用
doi:10.1038/s41467-017-01173-4

非小细胞肺癌是肺癌最常见的组织学类型,约占肺癌总数的 80-85%,近年来非小细胞肺癌发病率不断增高,无论是在我国还是全球,都已成为致死率最高的肿瘤。发表在《自然通讯》上的论文发现 YEATS2 基因在多种癌症细胞,尤其是非小细胞肺癌细胞中过量表达。研究者以非小细胞肺癌为研究体系,发现 YEATS2 基因敲低会明显抑制癌症细胞的增殖,随后的基因表达谱分析显示 YEATS2 可以上调一组核糖体编码基因(如 RPL7,PRL8,RPL35,RPL38 等)的表达,而这些基因对于维持细胞的正常生长十分重要。通过生化和结构生物学研究,李海涛课题组解析了 2.7 埃分辨率的 YEATS2 蛋白 YEATS 结构域特异性识别组蛋白 H3K27ac 的晶体结构,发现其 YEATS 结构域主要通过一种疏水的、丝氨酸内衬的三明治芳香笼口袋(S261、Y262、W282)实现对组蛋白 H3K27ac 侧链的精准识别,该识别涉及氢键、芳香 -π和碳氢 -π等相互作用,对其核心氨基酸进行突变则会明显减弱 YEATS 与组蛋白底物的结合能力。值得注意的是,YEATS2 存在于组蛋白乙酰转移酶 ATAC(Ada-Two-A-Containing)复合物中,该复合物可通过其催化亚基 GCN5 产生组蛋白 H3K9ac 修饰,从而提示一种从 H3K27ac 到 H3K9ac 的乙酰化放大机制。结合 ChIP-seq 和 ChIP-qPCR 分析,研究者们发现,ATAC 复合物和 H3K27ac 以及 H3K9ac 共定位于活跃转录基因的启动子区域,而 YEATS2 敲低明显减弱了 ATAC 复合物介导的下游靶基因(特别是核糖体基因)启动子区域 H3K9ac 的水平。进一步通过敲低 YEATS2 后过表达野生型 YEATS2 和阅读器口袋突变体,发现突变体无法挽救 ATAC 复合物依赖的核糖体基因的表达,同时也无法恢复癌症细胞的生长,从而证明了 YEATS2 对组蛋白乙酰化底物的识别对于非小细胞肺癌的发生、发展至关重要。
YEATS 结构域作为一类新型的组蛋白酰基化“阅读器”,其家族成员(YAF9,ENL,AF9,TAF14,SAS5 等)可形成多种复合物参与转录调控、组蛋白沉积、染色质重塑等过程。近年来,围绕 YEATS 家族蛋白识别组蛋白酰基化修饰的分子机制、及对其生物学功能的探索成为表观遗传领域的研究热点。该论文结合生物化学、细胞生物学、结构生物学等多种技术手段,展示了 YEATS2 通过介导组蛋白识别与催化而实现乙酰化信号放大的分子机制,并将 YEATS2 定义为一类促癌因子,为非小细胞肺癌等相关疾病的靶向治疗提供新思路。
10.Cancer Cell:科学家发现长期吸烟引起的肺细胞DNA表观遗传学变化或是肺癌发生的第一步
doi:10.1016/j.ccell.2017.08.006
近日,约翰霍普金斯大学研究人员给出了答案:香烟烟雾会导致细胞发生异常的DNA甲基化,进而使抑癌基因表达量下降,这会引起促进细胞生长的KRAS基因表达量升高,如果这个烟民的KRAS基因恰巧发生了致癌突变(1/3的吸烟肺癌患者携带这个突变),那么启动肺癌的第一步就这样开始了!
这项研究由约翰霍普金斯大学肿瘤学教授,Stephen Baylin,带领团队完成。最新的研究成果刊登在9月11日的著名学术杂志《Cancer Cell》上。
这些研究人员还发现只有暴露在烟草烟雾凝集物15个月的细胞(相当于人吸烟30年),在致癌突变的作用下,才能让小鼠长出肿瘤来,即发生致癌转化。而暴露在烟草烟雾凝集物6个月的细胞(相当于人吸烟12年),由于它的异常甲基化还不彻底,抑癌基因还可以发挥作用,所以即使是致癌的KRAS基因突变存在,细胞也不能发生致癌转化。
这些结果表明,慢性香烟烟雾暴露引起的早期表观遗传学变化,会随着时间的增加而增加,并且让人支气管上皮细胞对致癌的基因突变越来越敏感。它们和美国“癌症基因组图集”(TCGA)的数据分析结果不谋而合:与没有戒烟的人相比,戒烟10年以上的人的异常甲基化水平明显降低!
11.JNCI:周光飚研究组发现肺癌精准治疗新标记
doi:10.1093/jnci/djx157

动物研究所周光飚研究组系统研究了非小细胞肺癌中FAK的结构变异体。他们对91例肺癌病人的FAK基因组序列和编码区序列进行测序,发现在7例病人癌组织中存在4种类型的FAK变异体:一例病人发生基因内部串联重复突变体(FAK-ITD),一例病人发生A1004S点突变,一例病人发生第5-27号外显子缺失的突变,四例病人表达剪切异构体FAK6,7(在Y397自磷酸化位点前后分别插入编码6、7个氨基酸的外显子Box 6和Box 7)。与不吸烟病人相比,吸烟病人发生FAK变异的比例明显增高。分析癌症基因组测序TCGA数据库中肺癌病人的RNA测序数据,发现在508例肺腺癌病人中有42例 (占8.3%)、501例肺鳞癌病人中有37例 (占7.4%)病人表达含有“Box 6”及/或“Box 7”的 FAK可变剪切变异体,且吸烟的肺腺癌病例发生FAK结构变异的比例明显高于非吸烟病人。与野生型FAK相比, FAK-ITD和FAK6,7的自磷酸化水平增强(见图),酪氨酸激酶活性增高,对FAK激酶抑制剂的敏感性显著增强。该研究对肺癌病人FAK 抑制剂的临床精准应用具有指导意义,也说明吸烟可引起重要基因的剪切变异从而危害健康。 这一研究成果日前发表在Journal of the National Cancer Institute期刊上。





