病例摘要
47岁女性,有吸烟史(5包/年,7年前戒烟)。主要症状为咳嗽,左侧胸痛,诊断为社区获得性肺炎。胸部和腹部的CT扫描显示LLL病变,病理性淋巴结病变(左侧纵隔,左侧肺门和右侧锁骨上)以及肝脏病变。脑MRI没有明显颅内病变。
肿瘤类型:LLL病变的CT引导下活检显示NSCLC,肺腺癌。相关标记:CK7,TTF1,MOC-31和细胞角蛋白34βE12免疫染色阳性。初始分子研究:EGFR外显子18-21的测序未显示任何EGFR突变。ALK荧光原位杂交(FISH)阳性。67%ALK重排阳性。
讨论
➤针对ALK重排的常用检测方法有哪些?
➤针对这个患者可以采用什么样的治疗方案?
ALK阳性非小细胞肺癌是指包括ALK FISH检测、或ALK序列融合变异、或ALK融合蛋白IHC特定方法检测阳性的肺癌,是非小细胞肺癌的一个分子亚型,常见于腺癌,该类患者通常可从ALK抑制剂治疗中获益。
1.ALK测试有哪些可接受的方法?
肺癌中ALK变异主要为ALK基因发生重排与其他基因融合。其中,EML4-ALK(棘皮动物微管结合蛋白样4-间变性淋巴瘤激酶)融合基因变异是其主要类型,约占所有NSCLC的5%左右。
ALK可以与包括EML4,KIF5B和TFG在内的多种不同的配偶体基因进行重排,从而产生多种不同的转录物和融合蛋白。针对ALK靶点的小分子抑制剂Crizotinib(Crizotinib)是一种ATP竞争性酪氨酸激酶抑制剂,可特异性靶向抑制ALK激酶,也可抑制c-MET和ROS1等信号通路。CAP/IASLC/AMP选择肺癌患者进行EGFR和ALK酪氨酸激酶抑制剂分子检测指南于2013年7月发布(Lindeman,2013)。 2017年该指南将进行更新,预计将在今年晚些时候出版。更新后的指南重申并更新了2013年的大部分指南,并纳入了一些重要的新建议,包括检测所有肺腺癌患者的ROS1基因重排情况。
目前针对ALK融合基因检测常用的方法有三种——荧光原位杂交(FISH)、基于PCR扩增技术(RACE-PCR或RT-PCR联合测序技术、qRT-PCR等)和免疫组织化学法(IHC)。由于大量的配偶体基因和可能的重排,RT-PCR不是一种理想的筛选方法。ALK重排检测策略可能包括FISH,IHC,甚至下一代测序(NGS)。
FISH虽然是临床试验验证的标准方法,但价格昂贵,操作规范要求较高,且不能区分ALK融合变体(fusion variants)的类型;RT-PCR对标本取材要求较高,需专用的试剂盒进行检测;IHC简便易行,但阳性标准不统一。
大部分Crizotinib治疗ALK融合阳性NSCLC的临床试验均是基于FISH的诊断,因此,FISH检测目前仍是诊断ALK融合基因的参照标准方法。FDA已批准的雅培FISH分离探针试剂盒(Vysis ALK Break Apart FISH Probe Kit)可用于诊断ALK融合基因的表达。该试剂盒设计的两种探针分别标记ALK基因的两端,300 kb的3’端和442 kb的5’端分别标记为橘红色和绿色。在无ALK融合基因表达的肿瘤细胞中,橘红色和绿色重叠为黄色或者相互粘合(两个信号之间的间隔小于两个信号的直径);而在存在ALK融合基因表达的肿瘤细胞中,橘红色和绿色信号相互分离(间隔≥2个信号直径)。标本FISH阳性结果的判定标准为单个视野中的50个肺癌细胞中至少有25个存在分离信号,或者两个不同视野中的100个肺癌细胞中至少有15个存在分离信号。详细的FISH阳性判读标准可参见雅培ALK分离FISH探针试剂盒说明书。
ALK FISH技术适用的组织样本类型:10%中性福尔马林固定后石蜡包埋标本(FFPE样本),防脱玻片切片厚度3~5μm。
原位杂交技术检测ALK变异也存在不足之处。首先,FISH检测对于操作和判读技术要求较高,诊断医师必须经过严格的FISH操作和结果判读培训。只有经FISH操作经验丰富的医师判定的结果才具有可靠性。其次,晚期NSCLC患者通常只能提供2mm左右的小活检组织,很难保证每个视野均存在50个以上的肺癌细胞进行阳性判读。FISH检测结果的判断界值(cut off)也存在商榷之处,研究发现少数ALK FISH阴性、IHC阳性的患者能从靶向药物明显获益。最后,目前FISH检测的成本昂贵,且不能明确ALK融合基因的具体融合变体。因此,虽然FISH检测仍是诊断的重要手段,但现阶段尚无法适用于中国ALK阳性NSCLC患者的大规模筛查和诊断。
2.针对这个患者可以采用什么样的治疗方案?
2007年,肺癌患者首次检测到涉及编码ALK酪氨酸激酶基因的染色体重排(Soda,2007)。ALK重排在非小细胞肺癌中高达7%(Kris,2014)。 ALK重排的存在赋予对ALK抑制剂的敏感性(Kwak,2010)。Crizotinib是FDA批准的用于治疗ALK + NSCLC的标准方案。
与铂类化疗相比,第一代crizotinib已经在晚期ALK + NSCLC患者中显示出显着的活性,RR为74%,PFS为10.9个月(风险比为0.45)(Solomon and Mok,2015)。
第一代crizotinib是一种ALK / ROS1 / MET抑制剂,最初于2011年被美国FDA批准用于治疗晚期ALK + NSCLC。在两项随机III期试验(PROFILE 1014和PROFILE 1007)中,与一线和二线细胞毒性化疗相比,crizotinib分别使ORR,PFS和生活质量得到显着改善(Shaw,2013)(Solomon,2014)。与此例特别相关的是,在第一线crizotinib的PROFILE 1014试验中,与基于铂的化疗(Solomon和Mok,2015)相比,RR为74%,PFS为10.9个月(风险比为0.45)。基于这些研究,crizotinib成为晚期ALK阳性NSCLC的标准一线治疗药物。
虽然crizotinib已经改变了ALK + NSCLC的管理,但是2017年,还有一线ALK导向治疗的其他选择。
Ceritinib是第二代ALK TKI,具有增加的针对ALK的靶向活性(Mehra,2012)。基于ASCEND-1研究(Kim,2016)(Shaw and Engelman,2014),ceritinib最初是FDA批准用于一线crizotinib后发展为进展性疾病的患者。最近报道了ASCEND-4试验的结果(Soria,2017)。本研究将376例晚期治疗的ALK +肺癌患者随机分入ceritinib(189例)或铂 - 培美曲塞二联治疗(187例)。 Ceritinib组的中位PFS为16.6个月,而化疗组为8.1个月(HR 0.55,95%CI 0.42-0.73; P <0.0001)。使用ceritinib的中位缓解时间为23.9个月,化疗为11.1个月。值得注意的是,ceritinib的颅内反应率为57%,而化疗为22%。Ceritinib最常见的不良反应是腹泻,恶心,呕吐,疲劳和腹痛。
2017年5月,FDA扩大了对ceritinib适应证的批准,用于ALK阳性的转移性非小细胞肺癌(NSCLC)患者的一线治疗。
Alectinib是另一种第二代ALK TKI,其对ALK的靶向活性增加(Sakamoto,2011)。与ceritinib类似,根据两项单一研究(NP28673和NP28761)(Ou,2016)(Shaw,2016),alectinib最初是FDA批准用于一线crizotinib后发展为进展性疾病的患者。今年,在ASCO年会上,Global-ALEX研究的结果被提出,这项研究比较了alectinib和crizotinib的一线药物。本研究随机对303例晚期ALK + NSCLC患者进行alectinib或crizotinib治疗。中位PFS为alectinib为25.7个月,crizotinib为10.4个月。 12个月时,alectinib(9%)与crizotinib(41%)相比,脑转移的发生率更低。Alectinib最常见的不良反应是疲劳,便秘,肌肉疼痛和肿胀。
病例更新
该患者接受crizotinib治疗。1个月内症状好转,咳嗽减少,疼痛明显减轻。Crizotinib2周期后,CT扫描显示胸部和肝脏的肿瘤减小。占主导地位的左侧病灶尺寸从5.8×3.1厘米减小到4.6×1.7厘米。
该患者继续服用crizotinib14个月,此时间隔CT扫描显示肝脏有进行性疾病。
讨论
➤Crizotinib获得性耐药的机制是什么?
➤Crizotinib治疗后,二线治疗方案是什么?
尽管crizotinib初始反应良好,但大部分患者在治疗1年内耐药出现疾病复发,被称为获得性耐药。
1.Crizotinib获得性耐药的机制是什么?
Crizotinib耐药的机制与EGFR TKI相似,包括激酶结构域点突变,基因扩增和旁路信号通路激活。首个crizotinib获得性耐药的报道中,将一位接受crizotinib治疗复发后的腹水标本深度测序,结果提示两个不重叠的ALK酪氨酸激酶区域的突变,L1196M和C1156Y。体外实验提示以上任何一种突变都可以导致crizotinib的耐药。随后,其他ALK激酶区域的耐药突变在患者样本中陆续被发现,如G1269A、1151Tins、L1152R、1202R和1206Y。此外,ALK融合基因扩增在体内外已经被鉴定为耐药的原因。总之,大约三分之一的患者接受crizotinib治疗过程中复发是由于ALK耐药突变或ALK融合基因的扩增。第二种耐药机制为其他ALK相关信号通路的激活。体外研究提示,EGFR和`其他HER家族受体酪氨酸激酶能够通过配体介导激活ALK受体而导致耐药。此外,C-KIT基因扩增也可导致crizotinib耐药。其他潜在旁路机制包括EGFR和KRAS的激活突变等。
高达50%的第二代ALK抑制剂患者获得了ALK突变(G1202R,G1202 del,V1180L,S1206Y,E1201K等)(Gainor,2016)。值得注意的是,G1202R突变似乎是最顽固的。
肿瘤可能同时或逐步采用多种耐药机制,如何克服二线和三线的耐药是目前的挑战。
2.Crizotinib治疗后,二线治疗方案是什么?
目前已经开发了多个“第二”甚至“第三”代ALK抑制剂来尝试克服Crizotinib耐药性(表1)。这些“下一代”ALK抑制剂对ALK具有更高的靶向选择性和效力,并且与Crizotinib相比也具有更强的CNS渗透。这个领域的进展非常迅速,关于这个话题有很多信息。下面将重点总结那些已经获得监管部门批准的靶向药物。
表1 ALK抑制剂
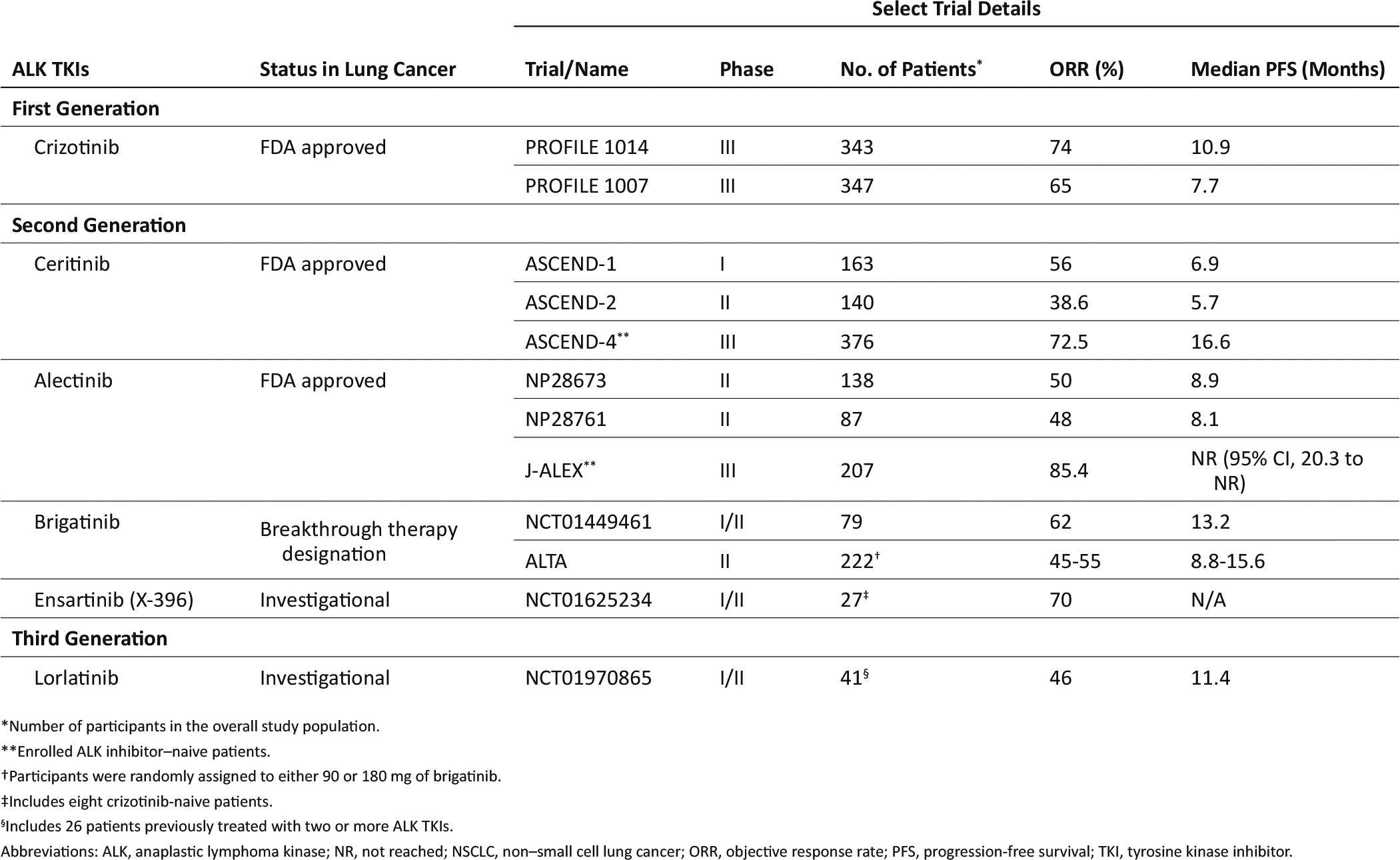
Ceritinib是FDA批准用于治疗Crizotinib耐药或不耐受的ALK阳性NSCLC。在两项研究中评估了Crizotinib耐药患者中的Ceritinib活性。
ASCEND-1是一项单独的I期试验,其中163名ALK抑制剂预处理的患者接受了ceritinib治疗(Kim,2016)。 ORR为56%,中位PFS为6.9个月。反应的中位数(DOR)为8.3个月。 75位患有脑转移的ALK抑制剂预处理患者中,颅内疾病控制率为65%。最常见的3-4级不良事件为腹泻(6%),恶心(6%),ALT升高(30%)和AST升高(30%)。
ASCEND-2是一项II期临床试验,140名接受ALK抑制剂预处理的患者接受了每天750毫克的ceritinib(Crino,2016)。所有患者都曾接受过Crizotinib治疗。 ORR为38.6%,中位PFS为5.7个月。中位DOR为9.7个月。颅内ORR为45.0%。最常见的AES主要是1级和2级,包括:恶心(81.4%),腹泻(80.0%)和呕吐(62.9%)。
Alectinib也被FDA批准用于Crizotinib耐药或不耐受的ALK阳性非小细胞肺癌的治疗。已经在两个单臂2期研究(NP28673和NP28761)中评估了alectinib对Crizotinib耐药的患者的活性。
对于NP28761研究,87例全部接受Crizotinib治疗的患者均接受Alectinib600 mg bid。 60%的患者有基线脑转移。 ORR为48%,PFS为5.7个月(Shaw,2016)。中位DOR为13.5个月。基线时16例可测量的中枢神经系统疾病患者的颅内ORR为75%。中枢神经系统反应的中位持续时间为11.1个月。最常见的AE(大多为1级或2级)分别为便秘(36%),疲劳(33%),肌痛(24%)和外周性水肿(23%)。最常见的3-4级不良事件是CPK升高(8%),ALT升高(6%),AST升高(9%)。
对于NP28673研究,先前接受crizotinib的138名患者接受600mg bid的Alectinib。 ORR为50%,中位PFS为8.9个月(Ou,2016)。中位DOR为11.2个月。基线时35例可测量的中枢神经系统疾病患者的颅内ORR为57%。中枢神经系统反应的中位持续时间为10.3个月。最常见的AE(大多为1级或2级)为便秘(33%),疲劳(26%)和外周性水肿(25%)。最常见的3-4级AE为呼吸困难(3%),ALT升高(2%)和AST升高(%)。
小结
1.目前针对ALK融合基因检测常用的方法有三种——荧光原位杂交(FISH)、基于PCR扩增技术和免疫组织化学法(IHC)。
2.新一代测序(NGS)正迅速融入常规实验室测试。
3.ALK TKI耐药机制多种多样,包括ALK激酶结构域突变,ALK扩增,EMT和SCLC转化。
4.四种不同的ALK TKIs已经被FDA批准用于ALK + NSCLC患者。
目前仅有10年的临床前报告记录了NSCLC患者中ALK重排的情况(Soda,2007),该领域发展迅速而且显着,到目前为止我们有强有力的证据显示,未来的鉴定和治疗以ALK为目标应该是治疗的标准。四种不同的ALK TKIs已经被FDA批准用于ALK + NSCLC患者,并且患者现在正在用多种ALK TKI疗法进行常规治疗。其他的ALK TKI也正在开发中,希望更多的患者获益。
参考文献
[1]Lung Cancer (August 2017): Molecular Oncology Tumor Boards.ASCO University.
[2]张绪超, 陆舜, 张力,等. 中国间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌诊断专家共识(2013版)[J]. 中华病理学杂志, 2013, 42(6):402-406.





