精准医疗如何对抗癌症?
时间:2017-09-11 09:49:58 来源:生物谷 点击:
1. Ultrasound Med Biol:杀伤癌细胞的"精准"化疗策略





癌症的治疗,包括化疗在内,能够帮助很多患者延长寿命以及提高生活质量。然而化疗也会对身体产生极大的副作用,这是由于化疗药物不仅能够杀伤癌细胞,还会对自体的健康细胞进行攻击。
而由于目前缺乏精确靶向癌细胞的疗法,因此仅有0.01%的化疗药物能够精确到达肿瘤组织进而杀伤。
最近,来自NTNU的研究者们开发出了一种新型的治疗癌症的精准疗法,目前小鼠水平的试验结果已经证明了该方法的可靠性。该文章的作者Sofie Snipstad博士称:"超声波能够提高靶向乳腺癌细胞的纳米颗粒包裹的药物的运输效果以及治疗效果",相关结果发表在最近一期的《Ultrasound in Medicine and Biology》杂志上。
Snipstad的方法能够将化疗药物靶向癌细胞,同时尽可能地不对健康细胞造成影响。目前该疗法已经在三阴性乳腺癌小鼠模型中进行了炎症。
与直接将药物注入血液不同,该方法选择了将药物包裹在纳米颗粒中。由于体积较大,这些颗粒在健康的组织周围只能停留在血管中,进而避免了其对健康细胞的伤害、而在肿瘤组织中,由于血管有很多孔状结构,因此纳米颗粒能够轻易地穿过血管进入组织。不过,由于纳米颗粒仅能够将药物运送到靠近血管的肿瘤组织,因此那些远离血管的肿瘤细胞无法受到药物的影响。
特别地,这些纳米颗粒能够形成微泡,而颗粒本身处于微泡的表面。当注入血液中之后,超声波将引导其破裂,从而能够帮助纳米颗粒的释放。这种"爆破"还能够导致血管出现更多的穿孔,进而方便药物进入肿瘤组织内部。
试验结果表明,上述方法向肿瘤组织中运输的有效药物浓度是常规方法的250倍,而且接受这种治疗方法的小鼠肿瘤的生长受到了更为明显的遏制。总之,这一技术为癌症的化学治疗提供了新的药物运送策略。

一项新的生物医学工具能够利用纳米颗粒运送基因到达靶细胞中,从而方便解决多种疾病,包括癌症、糖尿病以及HIV,这种方法相比传统的治疗手段更加快速、廉价以及便捷。
这一工具是由来自Fred Hutchinson癌症中心的研究者们开发出的。相关的前临床试验结果发表在最近一期的《Nature Communications》杂志上。
"我们的目标是将基于细胞的治疗手段变得更加简单化",该文章的作者,来自Fred Hutch 临床部门的生物材料学专家Matthias Stephan说道:"在这项研究中,我们开发出了一种新的产品,只需要将培养的细胞放进去就就能够达到治疗效果,而不需要任何其它的操作"。
Stephan等人开发的这种基于纳米颗粒的药物运输系统,能够扩大mRNA的治疗潜能,即能够将RNA直接运送到机体的细胞中,从而指导机体编码蛋白质抵抗疾病的发生。通过运送mRNA进行遗传调控,能够起到短期范围内的基因表达特征的改变,这种方式不会改变细胞中原有的遗传信息,从而避免对机体产生不可避免的影响。
Stephan等人利用三个例子证明其技术的可靠性:
首先,利用纳米颗粒携带T细胞基因编辑工具,从而对天然的T细胞受体进行改造,之后将其与编码"嵌合抗原受体(CAR)"的基因联合使用,从而使改造后的T细胞能够靶向肿瘤细胞发起攻击。
其次,纳米颗粒携带能够促进造血干细胞复制的mRNA,从而加快造血干细胞增殖的速率,并且通过骨髓移植的方式替换体内原有的癌细胞。
第三,纳米颗粒携带能够改造CAR-T细胞的mRNA以及foxo1mRNA,从而使得抗癌T细胞产生"记忆"能力,最终形成长期的抗癌属性。
目前这项技术仅仅在实验室水平得到了检验,并不一定适用于临床实践,但Stephan目前正在寻找商业伙伴,以促进该技术在临床中的应用。
doi: 10.7554/eLife.23421

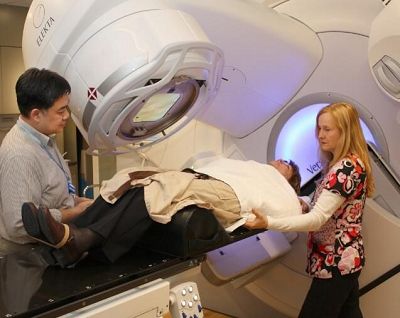
精准医疗如今越来越成为癌症疗法的创新性领域了,研究人员往往会对用普通药物进行治疗的患者进行靶向特殊肿瘤和分子的治疗,尽管目前研究者已经在靶向癌症疗法领域看到了进展,但未来仍然还有很长一段路要走;近日来自莫菲特癌症研究中心及达纳-法伯癌症研究所的研究人员利用非侵入性的方法评估肺部肿瘤的分子和临床特性,阐明了放射组学在改善精准化治疗上的潜力和作用,相关研究刊登于国际杂志eLife上。
放射组学能够为很多科学家及临床研究者提供新的方法来分析单个肿瘤的特性,从而指导癌症疗法,并且预测患者对疗法的反应;研究人员会通过多种方法对癌症患者的肿瘤进行成像,这些方法包括电脑断层扫描(CT)、磁共振(MRI)、正电子成象术(PET)等,肿瘤图像就能够帮助临床医生确定患者肿瘤的位置和阶段,从而指导疗法决策。这些图像或许能够用于放射组学领域来提取出高维数据帮助指导更为精准化的治疗;研究人员就能够利用放射组学来对肿瘤的不同特性进行定量,比如形状、尺寸、质地等,随后这些数据也能够同患者的遗传及临床数据结合帮助研究者更好地预测患者的临床预后及潜在的治疗手段如何对患者进行治疗。
研究者Robert Gillies博士表示,放射组学的核心理念就是图像并不是图片,而是数据;如今我们提取出了大约1300种不同的定量特性数据;研究人员随后对262名非小细胞肺癌的北美患者以及89名欧洲患者进行研究,分析患者的CT图像特性,随后研究者鉴别出了图像特性、分子标志物、生物学途径以及患者临床预后之间的关联;研究者表示,放射组学算法具有较强的临床重要性。
在指导精准化治疗上放射组学具有多种优势,目前研究者会侵入性地提取组织样本来分析生物标志物的特性,但常常这并不能准确反映整个肿瘤的生物学特性;相比较而言,成像技术却是非侵入性的,而且能够通过整个的治疗和反应过程来向研究者提供完整肿瘤的信息;此外,大部分的癌症患者通常都会进行用于诊断目的的图像,这就使得放射组学成为了一种成本效益的方法。
最后研究者Gillies表示,本文研究或能加速科学家们利用放射组学进行肿瘤特性的研究步伐,随着成像技术慢慢成为临床实践中的常规治疗标准,本文研究也将会为研究者提供新的机会来帮助改善患者的精准化治疗。
doi:10.1038/nature23306

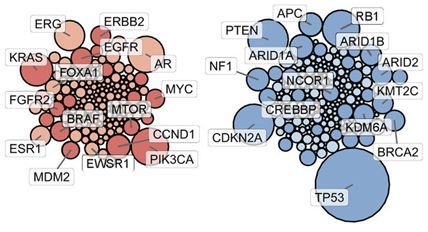
在一项新的研究中,来自美国密歇根大学、斯隆凯特林癌症纪念中心和霍华德-休斯医学研究所的研究人员发现,平均而言,转移性癌症具有的基因突变比在早期阶段的肿瘤中观察到的更多。相关研究结果于2017年8月2日在线发表在Nature期刊上,论文标题为"Integrative clinical genomics of metastatic cancer"。
这意味着为了使得精准医疗在癌症治疗中成为现实,你需要一种实时的综合方法来详细地研究转移性肿瘤和转移步骤。这种详细程度是最为常见的测试方法所不能够达到的。
作为对晚期癌症的基因特征和分子特征开展的最大规模和最为综合的研究之一,这些研究人员对500名转移性癌症患者的DNA和RNA进行测序。
这项研究的独特之处在于:(1)研究人员获得大多数患者的新鲜活组织,而且是从转移性肿瘤而不是从原发性肿瘤中提取样品;(2)他们对DNA和RNA进行测序;(3)他们对癌变组织的DNA与患者正常组织的DNA进行比较。
论文通信作者、密歇根大学转化病理学中心主任Arul Chinnaiyan博士说,"这种方法比大多数商业上获得的临床测序方法更加全面。我们的结果表明这种更加详细的方法在多种水平上都具有价值。"
这些数据反映了首批参与密歇根肿瘤学测序项目(Michigan Oncology Sequencing Program)的500名实体瘤患者。密歇根肿瘤学测序项目开始于2010年,对转移性癌症和正常组织的DNA和RNA进行测序以便鉴定出可能有助促进疗法开发的变化。该项目包括一个精准医疗肿瘤委员会,在这个委员会中,专家们讨论每个病例。Mi-ONCOSEQ是给癌症患者提供的首批综合临床测序项目之一。
这些患者涉及30多种癌症,并且肿瘤转移到22种不同的器官。尽管Mi-ONCOSEQ也适用于血癌患者和儿童患者,但是在这项新的研究中,它仅包括成年实体瘤患者。
对转移性肿瘤而不是对原发性肿瘤进行活组织取样
这些研究人员发现相比于患者的原发性癌症,在转移性癌症中发生的突变数量和类型显著增加。他们发现几乎每个转移性癌症病例含有更多的突变。这可能反映了转移性癌症更具侵袭性:转移性癌症有更多的机会产生进一步的突变,而且旨在杀死它们的疗法会导致更多的突变。
Chinnaiyan说,"我们的发现强调获得转移性肿瘤的新鲜活组织样品是比较重要的。肿瘤通过进化发生转移,需要接受治疗。我们需要获得转移性肿瘤的活组织,随后给出治疗建议,而不是利用来自原发性肿瘤的组织给出这样的建议。"
RNA测序揭示出更多的靶标
另一个关键的组成部分是对RNA和DNA进行测序。这种具有更加广泛应用的方法揭示出许多分子在肿瘤微环境中发挥着作用,促进和允许癌症继续生长、扩散或躲避治疗。
一般而言,大多数临床测序研究仅聚焦于DNA测序。尽管DNA测序揭示出参与转移性癌症的基因变化,但是这些研究人员发现RNA测序阐明了激活致癌基因或关闭阻止癌症产生的基因的内在机制。他们的发现可能有助鉴定出潜在的治疗靶标。
此外,通过研究RNA,这些研究人员能够研究肿瘤微环境中的免疫细胞,这会给为何免疫疗法可能仅适合治疗一些患者但不适合治疗其他患者提供线索。
Chinnaiyan说,"理解免疫微环境(immune microenvironment)---浸润到肿瘤中的细胞类型和它们正在表达哪些基因----是比较重要的。它让我们了解免疫表型(immuno-phenotype)。我们猜测我们可能利用这一点协助确定哪些患者对免疫疗法作出反应。"不过,在这个领域还需开展更多的研究。
另一个关键发现是转移性肿瘤表现出两个相互排斥的特征之一。一种特征是高度增殖,这意味着它侵袭性地增殖。在另一种特征中,细胞通过上皮-间质转化(epithelial to mesenchymal transition, EMT)丧失了分化能力。
Chinnaiyan说,"并不是所有转移性肿瘤都是一样的。不同的通路促进它们存在非常大的差异---是高度增殖还是发生更多的分化。这种相互排斥的性质是一项惊人的发现,这可能指导我们开发新的疗法。"
发现遗传性突变
还有一项惊人的发现是12%的转移性癌症患者携带遗传性突变。这大约是在所有癌症患者中可能期待的四倍。这些突变是通过比较肿瘤DNA和正常组织的DNA而被鉴定出的。
大约四分之三的这些突变与DNA修复过程相关联,而且几种现存的疗法旨在靶向这种DNA修复过程。
Chinnaiyan说,"在转移性癌症患者中,这种遗传性突变发生率是比较高的。一旦鉴定出这些突变,那么这些患者家庭中的其他人可能也携带这些突变,并且具有更高的癌症发生风险。"
在适当的情形下,家庭成员可能寻求遗传咨询或进一步的筛选。参与Mi-ONCOSEQ项目的患者接受了遗传咨询,而且如果存在遗传性突变,那么这种遗传咨询就应扩展到这些患者的家庭。
这些研究人员当前正在分析这首批患者的治疗结果。今年早些时候在美国临床肿瘤学会年度会议上发布的初步数据提示着在四分之三的患者当中,他们的肿瘤经测序后具有"可靶向的突变(actionable mutation)",这意味着存在靶向这种突变的疗法。迄今为止,总共有将近2300名患者参与Mi-ONCOSEQ项目。

近日,来自哥德堡大学的研究人员通过研究开发了一种新方法来更精准地检测抗癌药物的作用效果,这种方法或为后期研究人员对特殊药物治疗疾病疗效的评估提供了新的希望。
研究者Berglind Osk Einarsdottir博士表示,对于癌症患者而言,一些处方药通常无法治疗其疾病,而且还会产生一定的副作用;但我们开发的新方法或许能够早期地在药物开发阶段中使用,来帮助确定哪类患者会因药物而获益。这种方法能够鉴别出是否癌症患者会因特殊疗法而获益,而这是基于外科手术过程中患者肿瘤组织的活组织检查结果。
这项研究中,研究者在动物模型中追踪肿瘤的生长,同时还检测了动物模型对不同癌症药物的反应,整个实验基于肿瘤的生长速率,会花费数周至数月时间。这种新方法目前并未在瑞典医疗系统中使用,但研究人员能够进行相关实验来阐明该方法是否能够发挥作用以及未来患者是否需要利用这种方法进行疾病的治疗。
在一项子研究中,研究者揭示了33名癌症患者对抗癌制剂Karonudib的反应机制,Karonudib是最近卡罗琳学院开发的一种新型制剂。研究结果表明,三分之二的患者样本都能够对疗法产生反应;但问题在于,这些患者之间是否存在一些共通之处,比如DNA、机体代谢、蛋白表达等等;相关的研究结果或能帮助研究者更好地预测在哪类患者中药物能够真正抑制其机体的肿瘤,并且对癌细胞进行杀灭。
研究者指出,这或许与组织中所发现的突变并没有什么关系,他们所看到的或许也只是一种方式,即肿瘤对疗法会产生耐受性;当然有些肿瘤样本中蛋白的表达水平较高,其能够帮助细胞排斥药物的攻击作用,当然这或许也是一种癌细胞所产生的一种耐受性机制。最后研究者说道,未来我们或许有望利用这种新方法以患者为导向,来鉴别哪种抗癌药物能够给特殊患者带来最大药效;或许也可以以药物开发为导向,帮助鉴别哪类患者会因特殊的抗癌药物而获益,当然这都需要后期研究人员更为深入的研究才能够实现。
doi: 10.1038/leu.2017.93.

近日,来自意大利的科学家在自然旗下期刊Leukemia上发表了一项最新研究进展,他们发现一种组蛋白去乙酰化酶抑制剂能够选择性杀伤发生某个基因重排的B前体细胞急性淋巴细胞白血病(BCP-ALL),该研究为这种难治白血病亚型的治疗提供了新的潜在药物。
携带CRLF2和JAK2基因变异的白血病细胞存在JAK/STAT信号途径的异常,并且病人往往预后情况不好。HDAC抑制剂givinostat/ITF2357能够通过抑制JAK/STAT途径在全身型幼年特发性关节炎和骨髓增殖性肿瘤的治疗方面发挥作用。这些发现让研究人员意识到givinostat这种药物可能对发生CRLF2重排的BCP-ALL也有作用,目前这种白血病还没有有效的治疗方法。
在这项研究中,研究人员发现givinostat能够抑制发生CRLF2重排的BCP-ALL细胞系的增殖,并诱导细胞凋亡。与之类似,givinostat还可以杀死发生CRLF2重排的病人体内的白血病细胞,但是对正常的造血细胞没有影响。研究人员还发现在低剂量情况下,givinostat能够下调JAK/STAT信号途径中的基因表达,抑制STAT5的磷酸化。
研究人员在在体内实验中观察到givinostat能够显著抑制人源化肿瘤异种移植模型体内肿瘤的生长。重要的是,givinostat能够杀死抵抗ruxolitinib的细胞,增强目前所使用的化疗药物的作用效果。因此givinostat与传统化疗药物联合或代表了治疗这种难治白血病亚型的一种有效方法。最后,givinostat对癌细胞的选择性杀伤作用能够有助于降低药物强度,降低毒性和相关并发症。
综上所述,该研究发现givinostat这种HDAC抑制剂对发生CRLF2基因重排的BCP-ALL有选择性杀伤作用,为该疾病治疗找到一种潜在药物。
DOI:10.1016/j.ccell.2017.02.017

在最近发表在国际学术期刊Cancer Cell上的一项新研究中,来自密歇根大学的研究人员开发了一种新治疗策略,可以靶向大约一半前列腺癌中都会发生的基因变异。
当TMPRSS2和ERG这两个基因在染色体上发生重定位并且融合在一起,就会开启前列腺癌发育。但是开发靶向ERG的小分子抑制剂一直存在很大挑战性。
在这项研究中,研究人员利用大分子多肽来靶向ERG,他们在细胞系和动物模型中证明这种方法可以有效靶向并促进ERG融合蛋白的降解,对细胞正常功能几乎不会产生影响。
"靶向这个融合基因的表达产物是一个很大的挑战。我们从另外一个角度解决了这一问题。"文章作者Arul M. Chinnaiyan这样说道。
研究人员发现了一组多肽能够与ERG蛋白发生特异性相互作用。他们在能够产生融合基因产物的细胞系上检测了这组多肽,发现可以破坏ERG功能。在不产生这种融合基因产物的细胞中,这些多肽几乎不会对基因表达产生影响。他们还研究了这些多肽如何影响ERG调控的生物学过程。
但是研究人员面临的其中一个难题就是这些多肽降解得很快,持续时间不够长无法到达指定部位。因此研究人员开发了一些多肽类似物来解决正常多肽的降解问题,这些多肽类似物持续的时间可以更长。
研究人员还在动物模型上对这些多肽类似物进行了检测,结果表明这些多肽类似物能够抑制获得ERG融合蛋白的前列腺肿瘤的生长。在延长治疗时间之后,超过三分之一的小鼠肿瘤在一月后没有出现复发迹象。
"这是进行前列腺癌精准治疗的一个很好的例子:只有出现ERG基因融合的病人才适合这种药物。而ERG融合蛋白在前列腺癌中非常常见,因此这类药物一定会大放异彩。"Chinnaiyan这样说道。
这种多肽方法的一个弊端就是这样的大分子无法直接穿过细胞膜,这就意味着这些多肽还需要经过某种修饰或者通过某种运输方法来通过细胞膜。由于小分子药物能够轻易进入细胞并与靶点结合,因此在药物开发中比较受青睐。
研究人员接下来将会进一步分析这些多肽与ERG融合蛋白结合的三维结构,希望能够将这类分子进一步开发成抑制ERG的小分子。与此同时他们还将继续研究如何将多肽类似物做得更好。



