与《心房颤动:目前的认识和治疗建议—2015》相比,新版本有哪些变化呢?我们来梳理一下。
从大的章节方面看,2015版主要有房颤的分类和机制、病理生理及预后、临床评估、抗栓治疗、控制心室率、节律控制、特殊类型的房颤以及急性房颤发作的处理和治疗这八个章节;在新版本中,房颤的流行病学和危害、房颤的危险因素和合并疾病管理、房颤的外科和杂交手术治疗、起搏治疗与心房颤动、尚待研究明确的重要临床问题都作为独立章节进行了详细介绍,其他章节也有很多具体问题进行了更新,反映了近年来房颤领域的新进展和发展方向。
房颤的分类
新版本仍然按照发作频率和持续时间对房颤进行分类,即阵发性房颤(paroxysmal AF)、持续性房颤(persistent AF)、长程持续性房颤(long-standing persistent AF)和永久性房颤(permanent AF)四类。
表1 心房颤动(房颤)的分类
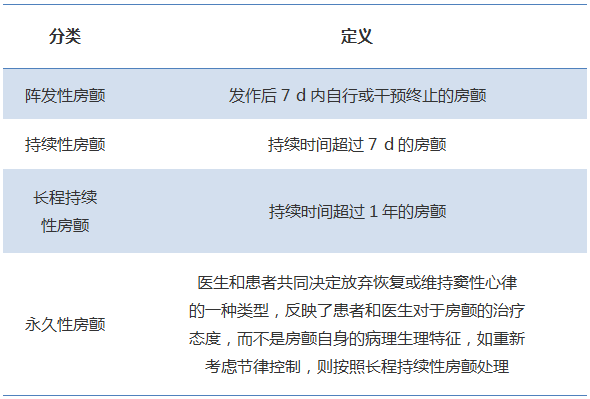
除了2015版中介绍的首诊房颤和非瓣膜性房颤,新版本还提到了沉默性房颤。沉默性房颤又称无症状性房颤(asymptomatic AF),是指没有临床症状的房颤。2017 HRS年会上公布的REVEAL AF试验结果提示,应关注高危患者中沉默性房颤的发病率和临床筛查。
房颤的临床评估
在病史采集和体格检查方面,新版本引用了《2014欧洲心律协会(EHRA)心房颤动的症状分类》建议使用的EHRA症状评分标准来评估房颤症状的严重程度。此外,还指出无症状性房颤也可导致卒中和死亡等严重后果。
表2 EHRA房颤症状评分标准

房颤的初始评估时,应重点关注血清电解质、肝肾功能、全血常规、甲状腺功能等实验室检查结果。
所有房颤患者初始评估时,均应常规行经胸超声心动图(TTE)检查来评估心脏结构、心房大小、左心室收缩功能、是否有附壁血栓等,从而指导临床治疗(Ⅰ,C)。当计划早期房颤复律时,行经食管超声心动图(TEE)检查排除心脏内血栓(Ⅰ,B)。TEE常用于指导房颤复律和射频消融治疗,还可发现血栓形成的高危因素。
对于存在脑缺血或卒中征象的房颤患者,行脑部CT或MRI检查,以检出脑卒中、指导急诊和长期抗凝治疗的决策(Ⅱa,C)。
关于房颤的筛查、监测和诊断,新版本认为,对于>65岁的患者,应通过心电图或触诊脉搏(对脉搏不规律的患者随后进行心电图检查)的方法筛查房颤;对于TIA或缺血性脑卒中的患者,应进行至少72 h连续的动态心电图检测(Ⅰ,B);建议对于脑卒中患者行长程无创心电监测或植入心电事件记录仪以发现无症状性房颤(Ⅱa,B);年龄>75岁或有高脑卒中风险的患者也可行长程心电监测以明确房颤的检出(Ⅱb,B)。
房颤患者的脑卒中预防
1.血栓栓塞和出血风险评估
对所有房颤患者应用CHA2DS2-VASc积分进行血栓栓塞危险评估(I,A);HAS-BLED评分能很好地预测房颤患者的出血风险。CHA2DS2-VASc评分≥2的男性或≥3的女性房颤患者应长期接受抗凝治疗(I,A)。一般情况下,对于依从性比较好的CHA2DS2-VASc评分为1的男性和为2的女性房颤患者也应接受抗凝治疗(Ⅱa,B)。
抗凝治疗应权衡风险和获益。出血和血栓具有很多相同的危险因素,出血风险增高者发生血栓栓塞事件的风险往往也高,这些患者接受抗凝治疗的临床净获益可能更大。因此,不应将HAS-BLED评分增高视为抗凝治疗的禁忌证,只要患者具备抗凝治疗的适应证仍需抗凝。
2.抗栓药物选择
在抗凝药物选择中,若无新型口服抗凝药物(NOAC)使用禁忌,可首选NOAC,也可选择华法林(I,A);不推荐单独的抗血小板治疗用于房颤患者血栓栓塞的预防(Ⅲ,A)。
(1)NOAC
NOAC的半衰期较短,预防房颤患者血栓栓塞事件的有效性与药物的依从性密切相关。对于已接受NOAC的患者,应定期复查肝肾功能,及时调整抗凝治疗方案。
表3 不同肾功能损伤患者使用NOAC的剂量推荐
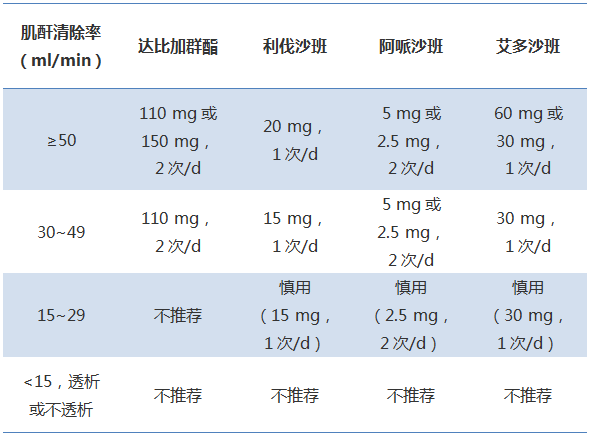
中度以上二尖瓣狭窄及机械瓣置换术后的房颤患者只能应用华法林进行抗凝;其他瓣膜疾病患者合并房颤时,应根据CHA2DS2-VASc评分确定是否需要抗凝,选用华法林或NOAC均可。
(2)华法林
接受华法林治疗时,目标INR为2.0~3.0,目前尚无证据显示国人需采用较低的INR目标值。建议尽可能使INR在2.0~3.0的时间(TTR)维持在较高水平(Ⅰ,A)。TTR<65%、或6个月内有2次INR>5.0或有1次INR>8.0、或6个月内有2次INR<1.5,均为INR不稳定。
华法林始用剂量2.0~3.0 mg/d,2~4 d起效,多数患者在5~7 d达治疗高峰。
INR在2.0~3.0范围内时华法林剂量不变,如超出范围则应调整华法林原服用剂量的10%~15%;若以往INR一直很稳定,偶尔出现INR增高的情况,若不超过3.5,可暂时不调整剂量,2 d后复查INR;在抗凝过度(INR>4.0)但不伴有出血的情况下,可停止给药1次或数次,一般在停用华法林3 d后INR会下降至治疗范围。
对应用华法林进行抗凝治疗的房颤患者,尽管已加强管理,如果TTR不能维持在较高水平,或患者倾向于服用NOAC,在没有禁忌证的情况下(如机械瓣)可改用NOAC(Ⅱb,A)。
3.导管消融围术期抗凝
术前已服用治疗剂量的华法林或NOAC,房颤导管消融围术期毋需中断抗凝(Ⅰ,A)。消融术中给予普通肝素抗凝时,应调整肝素用量以维持活化凝血时间(ACT)250~350 s(Ⅰ,B)。
射频消融术后推荐华法林或NOAC抗凝治疗至少2个月(Ⅰ,C);2个月后是否继续抗凝,取决于患者的脑卒中风险(Ⅰ,C)。
术前未进行系统抗凝或术前中断华法林或NOAC抗凝治疗者,应于术后止血后3~5 h启动抗凝治疗(Ⅱa,C)。消融术前未正规抗凝的房颤患者,术后如果采用华法林抗凝治疗,需在起始治疗时给予低分子肝素或普通肝素进行桥接(Ⅰ,C)。
4.经皮左心耳封堵
建议与2015版本基本相同,对于CHA2DS2-VASC评分≥2的非瓣膜性房颤患者,具有下列情况之一:①不适合长期规范抗凝治疗;②长期规范抗凝治疗的基础上仍发生血栓栓塞事件;③HAS-BLED评分≥3,可行经皮左心耳封堵术预防血栓栓塞事件(Ⅱa,B)。
心室率控制
房颤心室率控制包括急性心室率控制和长期心室率控制。房颤患者的最佳心室率控制目标值尚不明确,需根据患者的症状及合并症、心功能状态等情况个体化地确定。宽松心室率控制(静息心率<110次/min)可作为心室率控制的初始心率目标(Ⅱa,B)。
若血流动力学不稳定,可直接同步电复律(Ⅰ,B)。血流动力学不稳定或LVEF显著降低的患者,可考虑静脉使用胺碘酮以急性控制心室率(Ⅱb,C)。
LVEF≥40%的房颤患者,可选择口服β受体阻滞剂、非二氢吡啶类钙离子拮抗剂(维拉帕米、地尔硫䓬)或地高辛(Ⅰ,B);LVEF<40%的房颤患者,可选择口服β受体阻滞剂或地高辛(Ⅰ,B)。单一药物未能达到心室率控制目标时,可考虑联合药物治疗(Ⅱa,B)。

图1 房颤心室率控制的药物选择流程
推荐静脉使用β受体阻滞剂(艾司洛尔、美托洛尔)或非二氢吡啶类钙离子拮抗剂(维拉帕米、地尔硫䓬)用于急症但不伴有预激综合征房颤患者的心室率控制。预激合并房颤、妊娠合并房颤,节律控制而不是室率控制应作为首选管理方法(Ⅱa,C)。
对于心室率快速、症状明显,且药物治疗效果不佳,同时节律控制策略又不适合的患者可行房室结消融联合永久性起搏器植入以控制心室率(Ⅱa,B)。
节律控制
恢复和维持窦性心律的具体措施包括心脏复律、抗心律失常药物治疗和/或射频消融治疗。
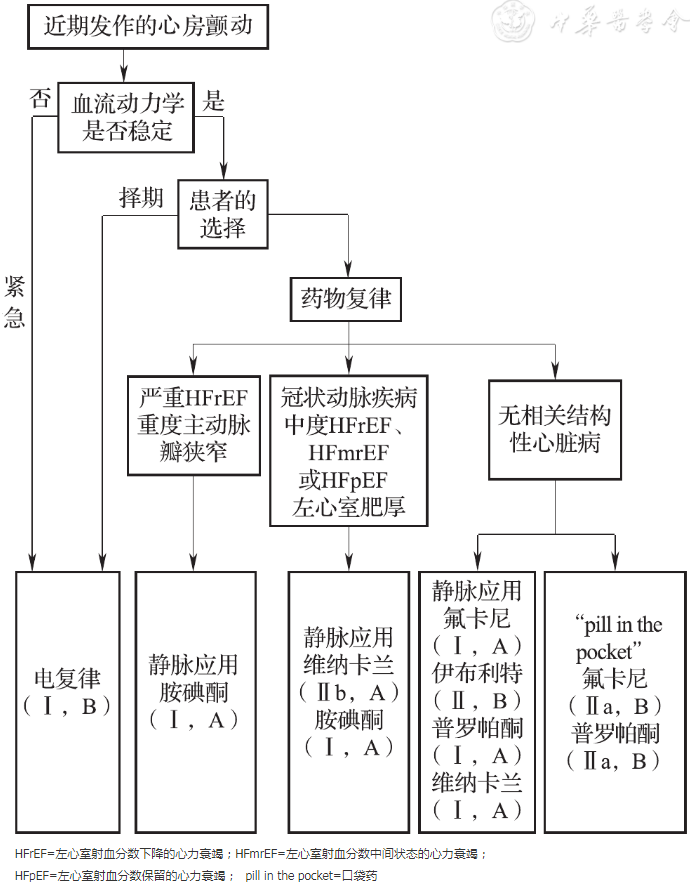
图2 近期发作的心房颤动节律控制治疗
1.药物复律
无缺血性或结构性心脏病病史的患者,推荐氟卡尼(Ⅰ,A)、普罗帕酮(Ⅰ,A)和伊布利特(Ⅱa,B);经选定的近期发作的房颤且无明显结构性或缺血性心脏病的患者,经安全性评价后,可考虑单次口服氟卡尼或普罗帕酮("口袋药"方法)用于患者自我复律(Ⅱa,B)。
缺血性和/或结构性心脏病患者,推荐胺碘酮作为房颤的复律药物(Ⅰ,A)。维纳卡兰可用于伴有轻度心衰(心功能Ⅰ级或Ⅱ级)、冠心病、左心室肥厚房颤患者的转律(Ⅱb,B)。
Ⅲ类推荐包括:①地高辛和索他洛尔用于药物复律(证据级别A);②院外应用奎尼丁、普鲁卡因胺、丙吡胺进行药物复律(证据级别B);③多非利特在院外使用(证据级别B)。
2.电复律
电复律可用于:①血流动力学不稳定的房颤患者(Ⅰ,B);②有症状的持续性或长期持续性房颤患者(Ⅰ,B)③预激综合征旁路前传伴快速心室率的房颤患者(Ⅰ,C)。
电复律前使用胺碘酮、氟卡尼、伊布利特或普罗帕酮增加电复律成功率并预防房颤复发(证据级别Ⅱa,B)。
3.复律后窦律的维持
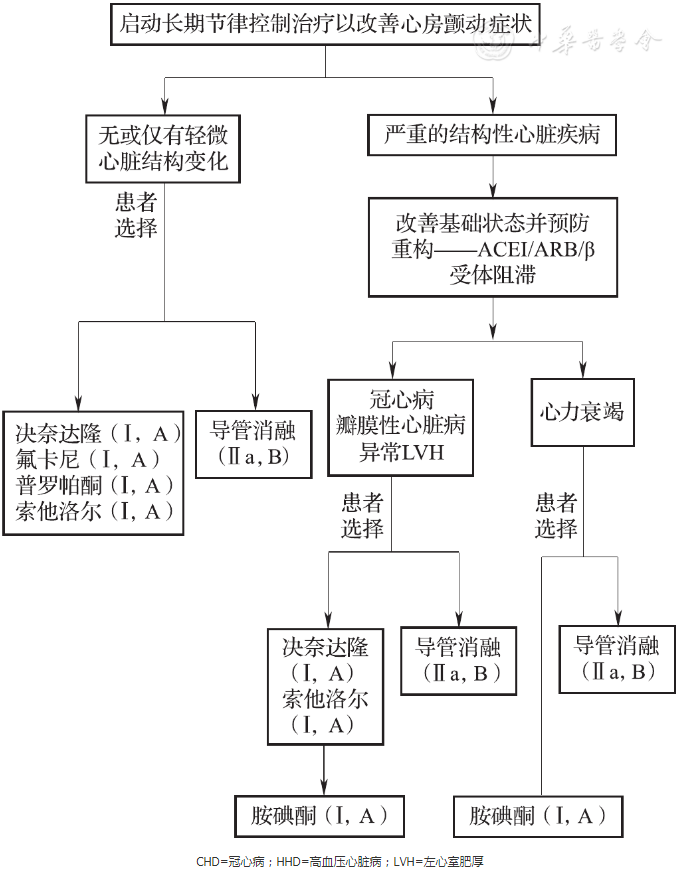
图3 在症状性心房颤动中启动长期节律控制治疗
(1)抗心律失常药物
预防左心室功能正常且无病理性左心室肥厚的症状性房颤的复发,可选氟卡尼、普罗帕酮、索他洛尔或决奈达隆(Ⅰ,A);预防无心衰的稳定性冠心病患者的症状性房颤的复发,可选决奈达隆(Ⅰ,A);预防心衰患者的症状性房颤的复发,可选胺碘酮(Ⅰ,B)。
在预防房颤复发方面,胺碘酮比其他抗心律失常药更为有效,但是其心外不良反应更常见且随时间而增加。因此,应首先考虑其他抗心律失常药物。
(2)非抗心律失常药物
心衰合并LVEF低的患者,可使用ACEI/ARB和β受体阻滞剂预防新发房颤(Ⅱa,A)。高血压,尤其是伴有左心室肥厚的患者,可使用ACEI/ARB和β受体阻滞剂预防新发房颤(Ⅱa,B)。
接受电复律并使用抗心律失常药物仍复发的房颤患者,可预防性应用ACEI/ARB治疗(Ⅱb,B)。
3.导管消融
症状性阵发性房颤患者,若经至少一种Ⅰ类或Ⅲ类抗心律失常药物治疗后效果不佳或不能耐受者,可行导管消融(Ⅰ,A)。
哪些患者可选择导管消融作为一线治疗呢?包括以下情况:
反复发作、症状性阵发性房颤患者,使用Ⅰ类或Ⅲ类抗心律失常药物之前,导管消融可作为一线治疗(Ⅱa,B);
症状性持续性房颤患者,使用抗心律失常药物治疗之前,权衡药物与导管消融风险及疗效后,导管消融可以作为一线治疗(Ⅱa,C);
对于职业运动员,考虑到药物治疗对运动水平的影响,导管消融可以作为一线治疗(Ⅱa,C)。
除此之外,存在下面的情况也可选择导管消融:
症状性持续性房颤患者,使用抗心律失常药物治疗后无效或不能耐受者,导管消融可作为合理选择(Ⅱa,B);
伴有心衰、肥厚型心肌病、年龄>75岁的房颤患者,在应用抗心律失常药物之前或之后均可考虑行导管消融,但须慎重权衡导管消融风险及疗效(Ⅱa,B);
伴有快慢综合征的房颤患者,导管消融可为合理治疗选择(Ⅱa,B);
症状性、长程持续性房颤患者,无论之前是否接受过抗心律失常药物治疗,权衡药物与导管消融风险及疗效后,均可行导管消融(Ⅱb,C);
一些无症状阵发性或持续性房颤患者,权衡导管消融风险及疗效后,均可行导管消融(Ⅱb,C)。





