高血压是导致残疾和心血管死亡的主要原因。长期以来,降压药物一直被视为将血压降至生理正常水平、预防高血压相关靶器官损害的主要方法。尽管已有有效的降压药物,但由于临床经验不足、耐药性明显等原因导致降压药物处方不合理,血压控制率仍然较低。
主要的循证临床指南从根本上使用标准的通用方法来为患者开具降压药物,但在个体患者层面上,这些方法并不是高度个性化的。临床实践表明,患者对降压药物的反应存在异质性。遗传多态性和药代动力学特征可能部分解释了个体间的用药差异性。越来越多的证据支持根据患者的遗传背景建立个体化药物治疗。

中南大学湘雅医院此前发布了基于药物基因组学的高血压个体化治疗临床队列研究,纳入长沙市9933名原发性高血压患者,分析抗高血压药物相关基因多态性的分布,并比较基因型指导和临床经验指导的高血压患者的临床疗效。研究表明,依据基因型指导用药的患者收缩压降低的程度、血压控制率增加的程度等显著高于临床经验指导用药的患者。因此,药物基因组学指导的高血压患者个体化治疗可能是一种更有效的策略。
高血压:心血管疾病重要危险因素
预防和控制高血压是遏制心脑血管疾病流行的核心策略
根据《中国心血管病报告(2018)》,我国心血管病现患人数约2.9亿,其中高血压2.45亿人,脑卒中1300万人,冠心病1100万人。
《中国心血管病一级预防指南(2020)》指出,心血管病是威胁我国居民生命和健康的重大公共卫生问题,每年导致死亡人数达400万,占总死亡的40%以上,也是伤残和寿命损失的重要原因。而高血压是导致我国居民心血管病发病和死亡的首要危险因素,约50%的心血管发病和20%的心血管病死亡归因于高血压。
研究表明,收缩压每降低10mmHg,或舒张压每降低5mmHg
-
死亡风险降低10%~15%
-
脑卒中风险降低35%
-
冠心病风险降低20%
-
心力衰竭风险降低40%
因此,预防和控制高血压是遏制我国心脑血管疾病流行的核心策略之一。
中国高血压流行特征
低知晓率、低治疗率、低控制率
《英国医学杂志》(BMJ)发表一项中国研究:中国居民慢性病与危险因素监测调查研究(CCDRFS)分别在2004年、2007年、2010年、2013年、2015年和2018年开展了6轮中国地区的普查,共近750万人次参与调查。研究表明,自2010年以来,中国高血压年龄标化患病率有所下降,虽然2004~2018年高血压知晓率、治疗率和控制率水平均有所提升,但整体水平仍较低。
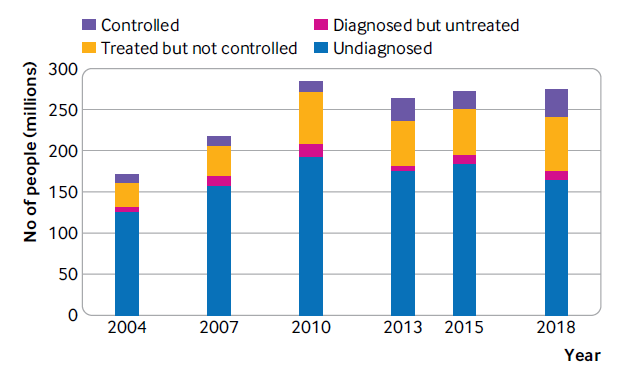
2004~2018年中国18~69岁成人高血压绝对负担变化趋势
(紫色指已经控制住的高血压,黄色指采取治疗措施但未能控制的高血压,红色指诊断为高血压但未治疗,蓝色指未确诊高血压)
降压治疗:艰辛的试药之路
遗传背景(基因)是影响降压药物疗效的重要因素
长期以来,降压药物一直被视为将血压降至生理正常水平、预防高血压相关靶器官损害的主要方法。尽管已有有效的降压药物,但由于临床经验不足、耐药性明显等原因导致降压药物处方不合理,血压控制率仍然较低。
当前降压治疗存在明显的个体差异,表现为部分患者疗效不佳或产生毒副反应。不同个体对于药物反应的差异性很大,影响因素包括年龄、并发症、营养状况、遗传背景、药物相互作用及环境等。其中遗传背景(基因)的影响尤为重要,越来越多的证据支持根据患者的遗传背景建立个体化药物治疗。
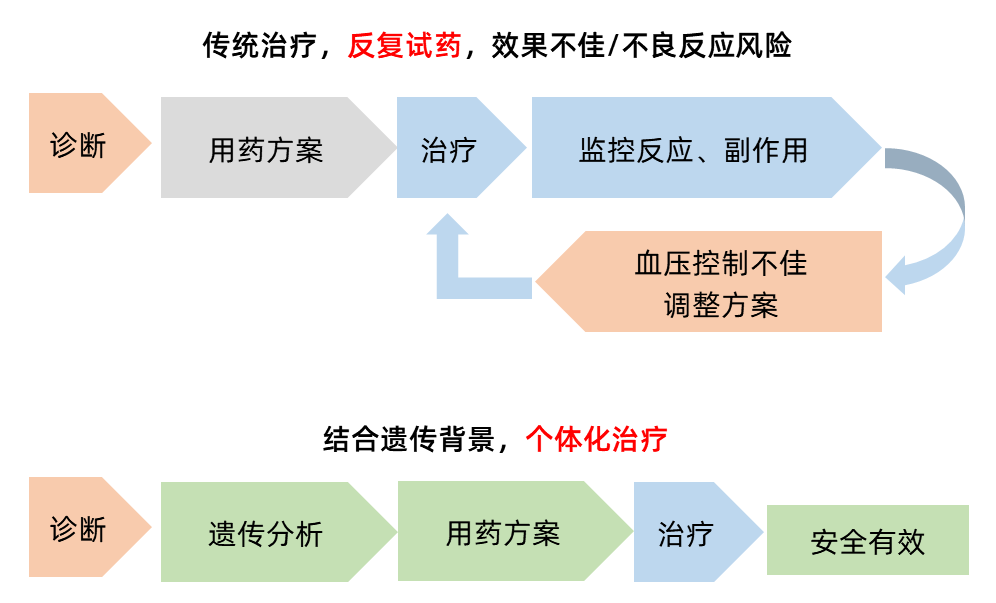
如何个体化应用降压药
药物基因组学(PGx)有利于高血压个体化用药
药物进入人体内,经过吸收、转运、代谢、效应及清除的过程发挥作用,个体由于基因的差异,导致药物在体内代谢、转运和作用靶点的遗传变异及其表达水平的差别,进而通过影响药物在体内浓度和敏感性等导致了药物疗效和毒性的个体差异。传统药物代谢动力学和药物效应动力学已经无法解释大多数药物影响的个体差异,药物基因组学(Pharmacogenomics, PGx)应运而生。
● 2013年,国家卫计委发布《医疗机构临床检验项目目录》,明确将高血压用药相关基因CYP2D6、CYP2C9、ADRB1、AGTR1、ACE的检测列入用药指导的分子生物学检验项目。
● 2015年,国家卫计委发布《药物代谢酶和药物作用靶点基因检测技术指南(试行)》,也推荐高血压用药相关基因检测项目,如CYP2D6*10多态性检测、CYP2C93多态性检测、ADRB1多态性检测、ACE(I/D)多态性检测等。
● 2015年,美国心脏协会、美国心脏病学院和美国高血压学会(ACC/AHA/ASH)联合声明:药物基因组学(PGx)有利于高血压个体化用药。
● 2017年,国家卫计委合理用药专家委员会及中国医师协会高血压专业委员会组织编写的《高血压合理用药指南(第2版)》明确提出:药物基因组学已经成为临床个体化用药的重要工具,高血压用药时应该考虑药物基因多态性的影响。
多中心、大样本的临床队列研究
基于药物基因组学的高血压个体化治疗是有效策略
此研究纳入了2017年至2018年湖南省长沙市乡镇卫生院和街道卫生服务中心登记的9933名26岁至96岁的高血压患者。从中抽取660名患者,按照3:1的比例随机分为2组,实验组根据基因检测调整降压药物治疗,对照组根据循证医学调整降压药物治疗。最终16例患者失访,实验组484例,对照组160例。
研究采集9933例高血压患者口腔黏膜基因样本,检测7个基因多态性位点(CYP2D6*10、ADRB1、CYP2C9*3、AGTR1、ACE、CYP3A5*3、NPPA),与ACEIs(血管紧张素转换酶抑制剂类) 、ARBs(血管紧张素受体阻滞剂类)、β受体阻滞剂、CCBs(钙拮抗剂类)和利尿剂等5种主要降压药物的代谢、转运和作用靶点相关,评估个体对药物的反应。根据不同个体的基因型和药代动力学特征,给予用药方案。
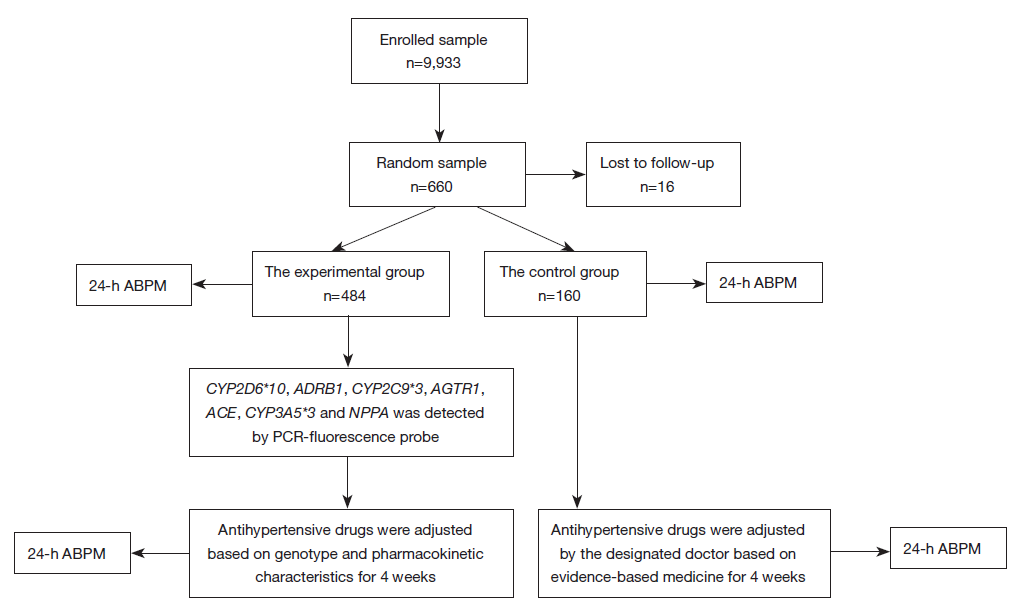
研究流程图
(ABPM,动态血压监测;PCR,聚合酶链式反应)
(1)患者对降压药物反应的异质性在很大程度上是由基因决定的;大部分高血压患者对β受体阻滞剂和CCB表现出更高的敏感性,对利尿剂的敏感性较差,而对ARB和ACEI的敏感性正常。开具上述药物处方时,应根据患者基因型和个体情况,适当调整剂量。
(2)实验组和对照组经过降压治疗后,舒张压均显著下降,实验组的收缩压下降有显著差异,对照组未达标的原因可能是根据临床经验调整的降压药物主要是降低舒张压,对收缩压的影响不显著。此外,两组血压控制率均显著增加,且实验组血压控制率增加幅度较对照组更为显著。这些结果表明,依据基因型指导的个体化治疗对高血压患者更有效,特别是对于收缩压显著升高的患者。
(3)临床上,高收缩压、低舒张压、脉压大是老年高血压患者的特点,收缩压与心脑血管事件独立相关。所以,基因型指导的降压治疗不仅可以为临床个体化用药提供新的科学依据,显著降低降压药物的副作用,还能够通过降低收缩压来降低高血压并发症的发生率。



